| DXA(デキサ)X線骨密度測定装置 お客様の声 DXAを用いた形状の異なるステム周囲の骨リモデリングの評価 |
|
| 【はじめに】 |
|
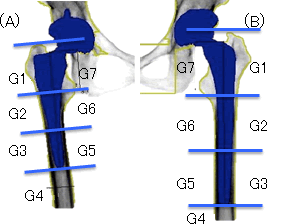
人工股関節周囲では荷重伝達が変化するため、骨リモデリングが起こる1,2)。今回、我々は異なる形状のステム周囲の骨リモデリングを評価したが、大腿骨側の骨リモデリングとしては、荷重伝達部位でおこるcancellous condensationと呼ばれる海綿骨の硬化像と、その近位でおこるstress shieldingによる骨萎縮が代表的である。Dual Energy X-ray Absorption (DXA)は骨密度を正確に測定する方法として有名だが、その応用として人工股関節周囲の骨リモデリング評価にも用いられている3–5)。 大腿骨の骨リモデリングの評価は一般的にはGruenのZone分類(図1)を用いて評価することが多い6)。GruenのZone分類ではステムの長さを3分割し、外側の近位からZone 1-3、ステム遠位端以遠をZone4、内側遠位からZone 5-7と設定している。Zone 1は大転子頂部まで含めるためやや長くなることがある。本稿では後に記載する等間隔Zone分類と区別するため、Zone1-7をG1-G7と記載する。GruenのZone分類はステムの長さに比例するため、図1に示すような形状や長さの異なるステムを比較する際に、骨の異なる部位において、異なる範囲を比較することになり、単純に比較することはできない。
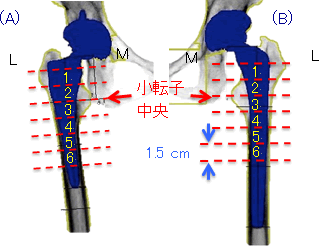
そこで当科では等間隔Zone分類(図2)を設定し、長さおよび形状の異なるステムの比較を行った。等間隔Zoneでは1.5cm幅のZoneを外側にL1からL6、また内側にM1からM6の6個のZoneをおいた。小転子中央を基準とし、M2とM3のZone間線がここに位置するようにした。これによりステム周囲の骨リモデリングを、骨の同じ部位において比較することが可能となった。
本稿では前半でGE Healthcare社、Lunar iDXAを用いた等間隔Zone分類の設定法を具体的に解説する。後半では等間隔Zone分類によって得られた結果について解説する。 |
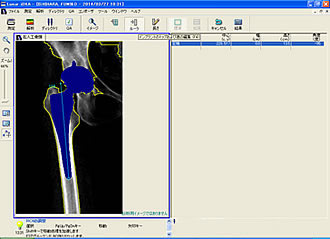
| 【Lunar iDXAを用いた等間隔Zone分類の解析法】 |
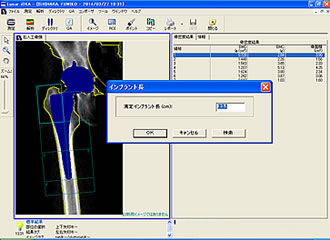
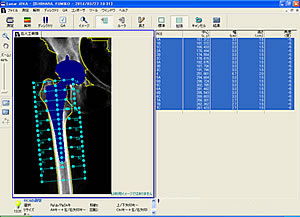
(2)ここでメニューバーの『ROI』アイコンをクリックすると、各Zoneの幅が4.5cmになる。メニューバーの『拡張』アイコンをクリックするとZone4以外の各Zoneが3分割され、1.5cmの等間隔Zoneが外側および内側に9つずつできる。この際にZoneの名前はGruenのZone分類に準じているため、外側では上から順に1A、1B、1C、2A、2B、2C、3A、3B、3Cとなっているが、内側では上からZone 7A、7B、7C、6A、6B、6C…となる。筆者の場合、Zone 7Cと6Aの間を等間隔Zone分類のM2とM3の間と決めて、そこを小転子の中央に合わせて等間隔Zone分類が出来上がる(図5)。小転子中央へのセットは、画面上でZoneの枠をドラッグし、マウス操作で調節する。
(3)Zone1Bから3Aが等間隔Zone分類のL1-L6に、Zone7B-5Cが等間隔Zone分類のM1−M6対応する。ここで注意を要するのは図5の右の表に載っているZoneの順番である。前述のように外側では1Aから3Cが上から順番に並ぶが、内側ではZoneが下から順に5、6、7となるのに対し、Zone内は上からA、B、Cとなるため7B = M1, 7C = M2, 6A = M3, 6B = M4と・・・画面上のZoneの順番と等間隔Zoneの順番が逆転する場所があるのでデータを入力する際に注意を要する。 (4)Zone幅の1.5cmという数値は、レントゲンにおいて小転子の大きさがおおよそ3cm前後となるため、M2が小転子上半分、M3が小転子下半分、それよりも近位はNeck、それよりも遠位は骨幹部となり、解釈しやすく、この値に決定した。 |
| 【形状の異なるステムへの等間隔Zoneの応用】 |
|
人工関節周囲の骨温存は再置換の際に重要である。Stress shieldingによる骨萎縮は直接的な有害事象ではないが、再置換時に問題となりうること、ステム周囲骨折の原因になる可能性があること、また、大腿部痛の原因となる可能性があることなど、潜在的な問題をはらんでいる7)。そのため、Stress shieldingによる骨萎縮を軽減することが望まれている。CentPillarステム(Stryker社、Mahwah、NJ, USA)は日本人の髄腔形状を解析して開発されたAnatomical short stemで、従来の近位型ステムより更に近位での荷重伝達が意図されており、近位でより骨温存されることが期待されている8–11)。 本研究ではCentPillarと従来型ストレートステム(Super Secur-Fit、Stryker社、Mahwah、NJ、USA)の骨リモデリングを比較するため、両側一期的THAにおいて片側にCentPillarを、対側にSecur-Fitを挿入した症例を対象とし、中期での骨リモデリングに対しDXAを用いた検討を行った。両側一期的THAにおける左右比較は、年齢や性別などを含めた個体差を最小限にすることができるため、比較的少ない症例数でステムの違いによる骨リモデリングの差を検討することができる11,12)。 対象は両側一期的THAにおいて片側にCentPillar、対側にSecur-Fitを挿入した34例である。手術時平均年齢50.9歳(31〜68歳)、 男/女=5/29、 診断:変形性股関節症 28例、特発性大腿骨頭壊死5例, 骨端異形成症1例。 評価は術後6-9年にGE Healthcare社、Lunar iDXAを用いて測定した骨密度をZone毎に評価した。統計処理は対応のあるt検定を用いておこない、p < 0.05を有意差とした。 GruenのZone分類を用い、骨密度を検討した。これ以降結果をSecur-Fit/CentPillar、P値の順に示す。G2(1.74 ± 0.28/1.56 ± 0.31、P<0.001)、G3(1.96 ± 0.23/1.85 ± 0.28、P=0.002)、G6(1.78 ± 0.26/1.52 ± 0.30、P<0.001)においてCentPillar側で骨密度が低かったが、図1に示すようにZoneの幅が異なるため直接的な比較は困難である。おそらくG2、G6に関してはCentPillar側で骨幹部の割合が少なく、関心領域における皮質骨の割合が少ないため、骨密度が低くなったと考えられる。 またG3は両側ともに骨幹部の領域であるが、CentPillar側はステム遠位部が細くなっているため、海綿骨の割合が高くなり、骨密度が低いという結果が得られたと考えられる。関心領域の面積と骨密度に関しては後に詳しく記載する。このようにGruenのZone分類では形状の異なるステムを比較した時に、骨リモデリングの違いを適切に評価することができない。DXAを用いた骨リモデリングの過去の報告では術直後と中期の骨密度を比較・評価をしている3–5)。しかしこれらにおいても形状の異なるステムの同部位の比較は不可能である。 そこで当科では等間隔分類を設定することで異なるステムの同部位の骨密度の比較を試みた。L3(1.16 ± 0.39/1.37 ± 0.35、P=0.001)、M3(0.85 ± 0.38/1.15 ± 0.34、P<0.001)、M4(1.70 ± 0.38/1.81 ± 0.34、P=0,036)においてCentPillar側で骨密度が高かった。この結果はCancellous condensationがSecur-Fit側では主にL4-L5およびM4-M5に認められたのに対し、CentPillar側ではL3-L4およびM3-M4に認められたことに対応しており、骨リモデリングの結果を反映していると考えられる。 本検討の限界として、ステムの形状が異なると関心領域の面積が変化することがあげられる。骨密度はX線の吸収によって見積もった骨量を関心領域の面積で割って得られる。ステム周囲の骨密度を検討する場合、ステムを除外して計算するため、ステムの形状(太さ)が異なると関心領域の面積、特に海綿骨の面積が変化する。そのため同じ等間隔Zoneにおいて関心領域の面積が異なると皮質骨と海綿骨の割合が変化し、見かけの骨密度が影響を受ける。例えばステムが細くなれば海綿骨の割合が増加し、見かけの骨密度が低下する。このように同じ部位で比較しても、関心領域の面積が異なると見かけの骨密度が変化するため、正確な比較が行えないことがわかる。 本研究のDXAにおける関心領域の面積は、近位(L1、L2、M1、M2)ではCentPillar側で有意に小さく、遠位(L5、L6、M4、M5、M6)ではCentPillar側が有意に大きかった。これは、CentPillarは近位の髄腔占拠率をあげるために嵩高くなっていることと、遠位では皮質骨との干渉を避けるために細く作られていることを反映しているためである。 本検討では前述のようにL3、M3、M4においてCentPillar側で骨密度が高いという結果が得られたが、少なくとも関心領域面積で差を認めなかったM3(1.63 ± 0.51/1.61 ± 0.46、P=0.871)に関しては信頼することができると考えられる。また、M4においてはCentPillar側で関心領域の面積が大きかったが(0.90 ± 0.24/1.01 ± 0.24、P<0.001)、この場合、海綿骨の割合が大きくなるため見かけの骨密度は低く見積もられるはずである。しかし、CentPillar側で骨密度が大きいという結果が得られたことから、M4においても有意な差と考えることができる。 |
| 【おわりに】 |
|
異なるステムを用いた人工股関節置換術後の骨リモデリングの差を、DXAを用いて検討することができた。ステムの形状が異なると関心領域の面積の違いによる誤差が含まれるため慎重な検討を要する。しかし、本研究において等間隔Zoneの>骨密度の結果はcancellous condensationの結果を再現しており、今まで定性的に議論していた内容を定量的に検討することが可能となった点において意義があると考えられる。 |
【引用文献】
-
1) Bobyn JD, Mortimer ES, Glassman AH, et al: Producing and Avoiding Stress Shielding. Clin Orthop Relat Res 274: 79–96, 1992.
2) Sychterz CJ and Engh CA: The Influence of Clinical Factors on Periprosthetic Bone Remodeling. Clin Orthop Relat Res 322: 285–292, 1996.
3) Rahmy AI, Gosens T, Blake G, et al: Periprosthetic bone remodelling of two types of uncemented femoral implant with proximal hydroxyapatite coating: a 3-year follow-up study addressing the influence of prosthesis design and preoperative bone density on periprosthetic bone loss. Osteoporos Int 15: 281–289, 2004.
4) Hirata Y, Inaba Y, Kobayashi N, et al: Comparison of mechanical stress and change in bone mineral density between two types of femoral implant using finite element analysis. J Arthroplasty 28: 1731–5, 2013.
5) Herrera A, Rebollo S, Ibarz E, et al: Mid-term study of bone remodeling after femoral cemented stem implantation: comparison between DXA and finite element simulation. J Arthroplasty 29: 90–100, 2014.
6) Gruen TA, McNeice GM and Amstutz HC: “Modes of Failure” of Cemented Stem-type Femoral Components. Clin Orthop Relat Res 141: 17–27, 1979.
7) Lindahl H: Epidemiology of periprosthetic femur fracture around a total hip arthroplasty. Injury 38: 651–4, 2007.
8) Noble PC, Kamaric E, Sugano N, et al: The Three-Dimensional Shape of the Dysplastic Femur. Clin Orthop Relat Res 417: 27–40, 2003.
9) Sugano N, Noble PC, Kamaric E, et al: The morphology of the femur in developmental dysplasia of the hip. J Bone Joint Surg Br 80: 711–719, 1998.
10) Jinno T and Yagishita K: What’s New in Orthopedics: Asian Perspective—Hip. In: Recent Advances in Orthopedics, 1st ed. Austin M and Klein G (eds.) JP Medical Publishers, New Dehli, India, pp202–214, 2014.
11) Miyatake K, Jinno T, Koga D et al: Comparison of Different Materials and Proximal Coatings Used for Femoral Components in One-Stage Bilateral Total Hip Arthroplasty. J Arthroplasty: in press, 2015.
12) Yamauchi Y, Jinno T, Koga D, et al: Comparison of Different Distal Designs of Femoral Components and Their Effects on Bone Remodeling in 1-Stage Bilateral Total Hip Arthroplasty. J Arthroplasty 27: 1538–1543, 2012.
※お客様の使用経験に基づく記載です。仕様値として保証するものではありません。
資料請求などのお問い合わせがございましたらこちらまで