
Innovation Talks
In GE HealthCare, l’innovazione è la chiave per trasformare il futuro. Da oltre 100 anni lavoriamo al fianco dei professionisti per sviluppare tecnologie all’avanguardia, dispositivi intelligenti e soluzioni che migliorano la cura dei pazienti. Con Innovation Talks, vogliamo aprire un dialogo sulle sfide e le opportunità che l’innovazione può offrire, ispirando il cambiamento e ridefinendo i confini dell’assistenza sanitaria.

Live Roundtable
Decodificare il cuore: oltre le immagini, verso il paziente
Tre casi clinici reali per affinare il percorso diagnostico e migliorare l'approccio al paziente cardiologico. Contattaci per ricevere i materiali.
Experience the conversation
Ascolta dalla voce degli esperti come l'avanzamento
tecnologico sta trasformando la pratica clinica
Nuove frontiere dell'imaging cardiovascolare: l'esperienza clinica del Dr. Piccoli
Nell'intervista, il Dr. Piccoli racconta come tecnologie TC di ultima generazione come Revolution Apex Elite stiano trasformando la gestione dei casi cardiovascolari complessi.

Intervista doppia
Caffè o tè? Il superpotere ideale? E il futuro dell’imaging cardiaco? Un radiologo e un cardiologo rispondono a domande inaspettate. Scopri cosa hanno da dire!
Dentro l'immagine
There is a world outside the stent mesh
Caso condiviso da Saima Mushtaq
Paziente con anamnesi di malattia coronarica e pregresso impianto di stent sulla discendente anteriore sinistra.
Per prima cosa, esamina l'intera scansione. Concentrati sul tronco comune e sulla porzione prossimale della discendente anteriore sinistra.
Fifty shades of grey
Caso condiviso da Marcello De Santis
Casi clinici
Scopri come le tecnologie di imaging più innovative di GE HealthCare hanno giocato un ruolo chiave nella diagnosi di condizioni cardiache complesse.

Luigi Badano
FESC, FACC, MD, PhD, Direttore dell'Unità di Imaging Cardiovascolare presso Istituto Auxologico Italiano, IRCCS, Ospedale San Luca, Milano
Uomo di 66 anni, anamnesi patologica remota negativa. Nessun fattore di rischio cardiovascolare

Denisa Muraru
FESC, FACC, MD, PhD, Istituto Auxologico Italiano, IRCCS, Ospedale San Luca, Milano
Paziente maschio di 53 anni con Cardiomiopatia Ipertrofica (HCM) e ostruzione apicale-medio-ventricolare (MVO)
Saima Mushtaq
Direttore dell'Unità Semplice di TC Cardiovascolare Centro Cardiologico Monzino IRRCS, Milano
Uomo di 52 anni con cardiomiopatia dilatativa e ICD per tachicardia ventricolare...

Marcello De Santis
Medico Radiologo presso Diagnostica per Immagini, IRCCS San Raffaele, Roma
Donna di 55 anni, con recente MINOCA, è stata sottoposta a risonanza magnetica cardiaca...
Gianluca Pontone et al.
Direttore Dipartimento Cardiologia peri-operatoria e Imaging cardiovascolare Centro Cardiologico Monzino IRRCS, Milano
Donna di 65 anni con ipertensione e storia di coronaropatia (CAD) trattata con stent su LAD, D1 e LCX...

Marcello De Santis
Medico Radiologo presso Diagnostica per Immagini, IRCCS San Raffaele, Roma
Uomo di 75 anni con cardiopatia ischemica cronica (CAD), è stato recentemente sottoposto a intervento...

Saima Mushtaq et al.
Direttore dell'Unità Semplice di TC Cardiovascolare Centro Cardiologico Monzino IRRCS, Milano
Un uomo di 80 anni con ipertensione e storia di CAD con stent su LAD e LCX...

Azienda ospedaliero-universitaria Sant'Andrea
Paziente di 42 anni con storia di dolore toracico esegue angiografia coronarica e analisi genetica, scopre la mutazione genetica MYH7...

La velocità di progressione della fibrosi cardiaca: un nuovo orizzonte
La velocità di progressione della fibrosi cardiaca emerge come un nuovo e cruciale indicatore prognostico nella cardiomiopatia ipertrofica. Un recente studio evidenzia come l’LGE rate sia più predittivo degli eventi avversi rispetto alla semplice estensione della fibrosi, aprendo nuove prospettive per il monitoraggio e la gestione terapeutica dei pazienti.
1-Beat Cardiac migliora la qualità diagnostica dell’angio-TC coronarica
L’angio-TC coronarica (CCTA) è uno strumento diagnostico essenziale per l’identificazione delle malattie coronariche, ma la sua affidabilità può essere compromessa nei pazienti con frequenza cardiaca elevata. Grazie ai progressi tecnologici, la modalità 1-Beat Cardiac consente ora di ottenere immagini di alta qualità anche in condizioni di elevata frequenza cardiaca.

ExpertConnect LIVE!
Hai mai desiderato confrontarti direttamente con un esperto per approfondire un caso clinico o i benefici delle applicazioni più avanzate in ambito diagnostico?
Con ExpertConnect LIVE, puoi farlo! Collegati alla macchina virtuale, esplora le immagini nei minimi dettagli e ottieni risposte su misura per la tua pratica quotidiana.

Imaging Cardiaco
La velocità di progressione della fibrosi cardiaca
La velocità di progressione della fibrosi cardiaca emerge come un nuovo e cruciale indicatore prognostico nella cardiomiopatia ipertrofica. Un recente studio evidenzia come l’LGE rate sia più predittivo degli eventi avversi rispetto alla semplice estensione della fibrosi
La cardiomiopatia ipertrofica (HCM) è una malattia del muscolo cardiaco
caratterizzata
dall'ispessimento delle pareti del cuore, che può portare a gravi complicanze, tra cui
aritmie pericolose e
morte cardiaca improvvisa. Una delle caratteristiche distintive di questa patologia è la
presenza di fibrosi miocardica, ovvero la formazione di tessuto cicatriziale
all'interno del muscolo cardiaco, che può
essere rilevata attraverso la risonanza magnetica cardiaca (CMR) con una tecnica
chiamata late adolinium enhancement (LGE).
Studi precedenti hanno dimostrato che l'estensione della fibrosi, quantificata tramite
LGE, è associata a
un peggioramento della prognosi nei pazienti con HCM. Tuttavia, una ricerca pubblicata
sull' American
Journal of Cardiology ha recentemente evidenziato come non sia solo la quantità
di fibrosi a essere
rilevante, ma anche la velocità con cui essa progredisce nel tempo.
Nello studio Prognostic Role of the
Progression of Late Gadolinium Enhancement in Hypertrophic Cardiomyopathy ¹, 105
pazienti con HCM (72 uomini, età media 53 anni) sono stati sottoposti a due
esami CMR, uno al basale (CMR-I) e un secondo dopo almeno due anni (CMR-II). Questo
approccio ha consentito ai ricercatori di calcolare il cosiddetto LGE rate, ovvero
l'incremento della fibrosi nel tempo, espresso in grammi al mese. L'obiettivo principale
era valutare se
questo parametro potesse fornire indicazioni prognostiche più precise rispetto alla
semplice misurazione
dell'estensione della fibrosi in un singolo momento.
I risultati hanno rivelato che la percentuale di pazienti con una fibrosi estesa (LGE
≥15% della massa ventricolare sinistra
) è aumentata significativamente nel tempo, passando dal 9% al 20%
tra il primo e il secondo esame di CMR (p = 0.03). Questo dato suggerisce come la
HCM non sia una
malattia statica, ma possa evolvere e peggiorare anche in pazienti con una condizione
apparentemente
stabile. In particolare, l'incremento della fibrosi è stato maggiore nei pazienti che al
CMR-I
avevano un LGE 15% e che al CMR-II hanno superato tale soglia. L'incremento
mediano di
questo gruppo è stato di 17 grammi (range interquartile da 9 a 26) contro 1
grammo
(range interquartile da 0 a 3) (p=0.04) dell’altro gruppo.
L'aspetto più innovativo dello studio è l'identificazione dell'LGE rate come fattore
prognosticoindipendente
per prevedere eventi avversi maggiori in pazienti con cardiomiopatia ipertrofica (HCM).
I
pazienti con un LGE rate superiore a 0.07 g/mese hanno mostrato un rischio
significativamente più
elevato di tali eventi rispetto a quelli con una progressione più lenta della
fibrosi.
Questo cut-off di 0.07 g/mese non è un numero casuale, ma è stato determinato
attraverso un'analisi
statistica specifica (MaxStat Analysis) che ha identificato questo valore come il
miglior predittore di
eventi avversi, con una sensibilità dell'84% (range dal 64% al 96%) e una specificità
dell'80% (range dal
70% all'88%). Inoltre, l'LGE rate 0.07 g/mese ha permesso una significativa
riclassificazione netta del rischio dei pazienti rispetto al parametro LGE ≥15%
in un singolo punto temporale,
sia al primo che al secondo esame (CMR-I NRI 0.49, 95% CI 0.16 to 0.82, p = 0.003 vs
CMR-II NRI 0.27, 95% CI 0.02 to 0.52,
p = 0.03). Ciò significa che la progressione della fibrosi, misurata attraverso l'LGE
rate, è un indicatore che,
se confermato anche da altri studi con coorti più numerose, potrebbe essere più preciso
e utile per
identificare i soggetti a maggiore rischio rispetto alla misurazione statica dell’LGE.
Le implicazioni cliniche di questa ricerca sono rilevanti. Innanzitutto, lo studio
suggerisce che la
CMR andrebbe ripetuta in tutti i pazienti con HCM (in un periodo che potrebbe essere
variabile tra 2-5 anni,
alla luce della presenza di “rapidi e lenti progressori” documentati in
Letteratura), soprattutto in quelli
con una LGE inferiore al 15% al basale. Questo approccio consentirebbe di monitorare
l'evoluzione della
fibrosi e di individuare precocemente i soggetti che potrebbero andare incontro a un
peggioramento
della loro condizione.
Inoltre, la misurazione dell'LGE rate (ed eventualmente, se confermato con lavori
mirati, anche la
variazione del volume extracellulare con tecnica di T1 mapping ECV) potrebbe
nell’immediato futuro
contribuire a una stratificazione del rischio più accurata, consentendo di
prendere decisioni
terapeutiche più mirate, come l'impianto di un defibrillatore (ICD) nei pazienti a
rischio più elevato.
È importante notare come i meccanismi alla base della progressione della fibrosi non
siano ancora
completamente chiari. Tra i fattori ipotizzati vi sono ripetuti episodi di ischemia,
causati da una ridotta
perfusione del muscolo cardiaco, e alterazioni energetiche delle cellule cardiache.
Tuttavia, le terapie
convenzionali per la HCM, come i beta-bloccanti, non sembrano in grado di influenzare
significativamente la progressione della fibrosi, essendo efficaci prevalentemente come
“sintomatici”.
Questo apre la strada allo studio di nuove terapie, come i farmaci inibitori
della miosina, che potrebbero
agire direttamente sui meccanismi patofisiologici alla base della fibrosi.
Questi risultati sottolineano l'importanza di considerare la progressione della
fibrosi nella gestione
clinica della HCM. L'LGE rate si configura come un nuovo e promettente indicatore
prognostico,
potenzialmente in grado di migliorare la stratificazione del rischio e guidare le scelte
terapeutiche nei
pazienti affetti da questa complessa patologia.
In sintesi, questo studio apre nuove prospettive nella gestione della HCM, evidenziando
come la velocità
di progressione della fibrosi, misurata tramite l'LGE rate, sia un fattore prognostico
estremamente
importante. La ripetizione della CMR a intervalli regolari e l'attenzione alla
progressione della fibrosi
rappresentano elementi chiave per migliorare la cura e la prognosi dei pazienti affetti
da questa
malattia.
- Aquaro GD, Todiere G, Barison A, Grigoratos C, Parisella ML, Adami M, Grilli G, Pagura L, Faggioni L, Cioni D, Lencioni R, Emdin M, Neri E. Prognostic Role of the Progression of Late Gadolinium Enhancement in Hypertrophic Cardiomyopathy. Am J Cardiol. 2024 Jan 15;211:199-208. doi: 10.1016/j.amjcard.2023.11.003. Epub 2023 Nov 8. PMID: 37949342

Imaging Cardiaco
1-Beat Cardiac migliora la qualità diagnostica dell’angio-TC coronarica
Grazie ai progressi tecnologici, la modalità 1-Beat Cardiac consente ora di ottenere immagini di qualità elevata anche in condizioni di elevata frequenza cardiaca.
L’angio-TC coronarica (CCTA) è fondamentale per la diagnosi delle malattie
coronariche, ma
la sua efficacia può risultare compromessa nei pazienti con frequenza cardiaca elevata
(≥80
bpm), in quanto il movimento cardiaco e la variabilità del ritmo possono generare
artefatti
che riducono la qualità delle immagini. Questi pazienti, spesso ricoverati in pronto
soccorso
per dolore toracico acuto e sospetto di sindrome coronarica acuta, presentano un quadro
clinico in cui una diagnosi rapida e accurata è essenziale.
Tradizionalmente, l’elevata frequenza cardiaca ha rappresentato un limite all’esecuzione
della CCTA, a causa degli artefatti da movimento che ne compromettevano l'accuratezza
diagnostica. Tuttavia, grazie ai progressi tecnologici, come l'introduzione della
modalità
1-Beat Cardiac su Revolution CT/Apex, è ora possibile ottenere immagini di
alta qualità anche
in pazienti con una frequenza cardiaca superiore agli 80 bpm, senza compromettere la
sicurezza del paziente o esporlo a dosi eccessive di radiazioni.
Uno studio condotto da Andreini et
al.
ha valutato la performance diagnostica della Unlimited 1-Beat CCTA in un gruppo
di 202 pazienti,
di cui 100 con una frequenza cardiaca ≥80 bpm (età media: 64 anni; BMI medio:
27.4 kg/m²; frequenza cardiaca media: 93
bpm) e 102 con una frequenza ≤65 bpm (età media: 68 anni; BMI medio: 26.4 kg/m²;
frequenza cardiaca media: 57 bpm). L’obiettivo dello studio era confrontare
la qualità delle immagini e l’accuratezza diagnostica tra i due gruppi, valutando
la capacità della
tecnologia di rilevare stenosi coronariche superiori al 50%.
I risultati hanno mostrato che, nonostante la frequenza cardiaca più elevata,
la qualità delle immagini nel gruppo con frequenza cardiaca ≥80 bpm non era
significativamente
diversa rispetto a quella del gruppo con frequenza cardiaca inferiore (HR ≤65
bpm). In
entrambi i gruppi, la qualità è stata valutata come alta, con punteggi medi di 3.35 e
3.39 su
una scala Likert a 4 punti, e la percentuale di interpretabilità dei segmenti coronarici
è stata
quasi identica (97.3% nel gruppo con frequenza cardiaca alta e 98% nel gruppo con
frequenza cardiaca bassa).
La CCTA ha inoltre dimostrato di essere altrettanto precisa nel
rilevare una stenosi superiore al 50%, sia nei pazienti con frequenza cardiaca alta
che in quelli con
frequenza bassa. I valori di sensibilità, specificità e accuratezza erano molto
simili in
entrambi i gruppi, a conferma che la tecnica 1-beat Cardiac permette di mantenere
un’elevata accuratezza diagnostica indipendentemente dalla frequenza cardiaca.
Un ulteriore vantaggio della modalità 1-Beat Cardiac risiede nella riduzione significativa della dose di radiazioni. Studi precedenti avevano dimostrato che è possibile ottenere una buona qualità dell’immagine utilizzando sistemi TC a doppia sorgente con 128 strati, ma ciò comportava un’esposizione alle radiazioni relativamente elevata (dose media superiore a 20 mSv). Al contrario, lo studio di Andreini et al. ha evidenziato che l'uso della tecnica Unlimited 1-Beat Cardiac su Revolution CT/Apex ha permesso di ridurre significativamente la dose, mantenendola a una media di 2.9 mSv nei pazienti con frequenza cardiaca alta, rispetto agli 1.1 mSv nel gruppo con frequenza cardiaca bassa. Questo risultato è stato ottenuto grazie alla capacità di acquisire i dati in una finestra temporale di 500 ms, corrispondente alla fase tra la fine della sistole e la fine della diastole, in un unico ciclo cardiaco.
- Andreini D, Mushtaq S, Pontone G, Conte E, Guglielmo M, Annoni A, Baggiano A, Formenti A, Ditali V, Mancini ME, Zanchi S, Melotti E, Trabattoni D, Montorsi P, Ravagnani PM, Fiorentini C, Bartorelli AL, Pepi M. Diagnostic performance of coronary CT angiography carried out with a novel whole-heart coverage high-definition CT scanner in patients with high heart rate. Int J Cardiol. 2018 Apr 15;257:325-331. doi: 10.1016/j.ijcard.2017.10.084. PMID: 29506722
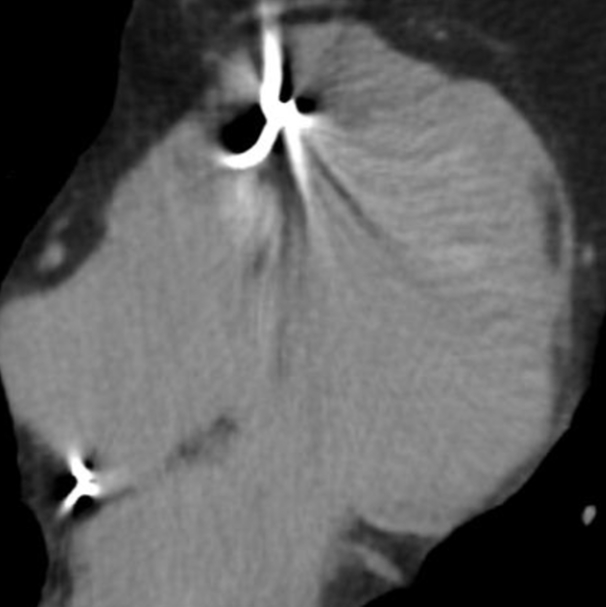
Imaging Cardiaco
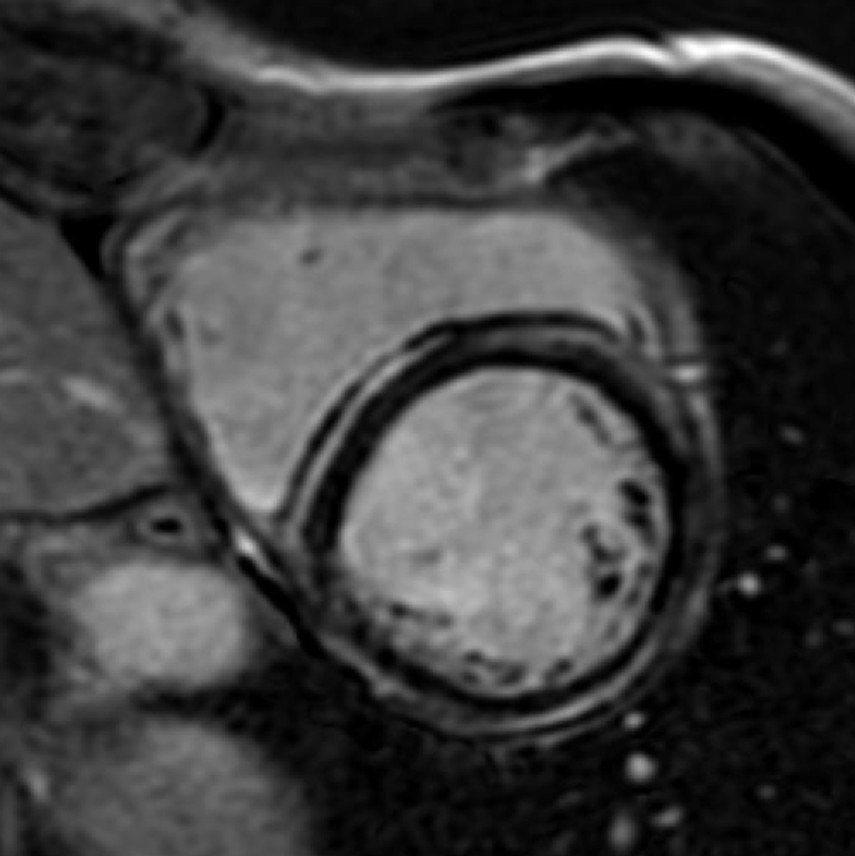
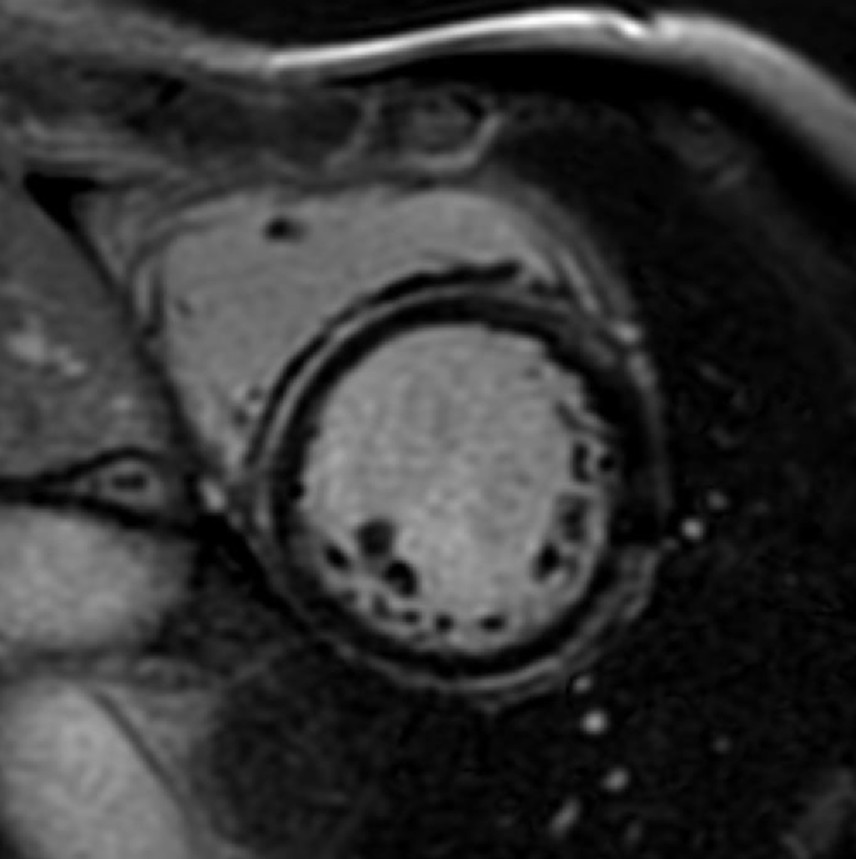
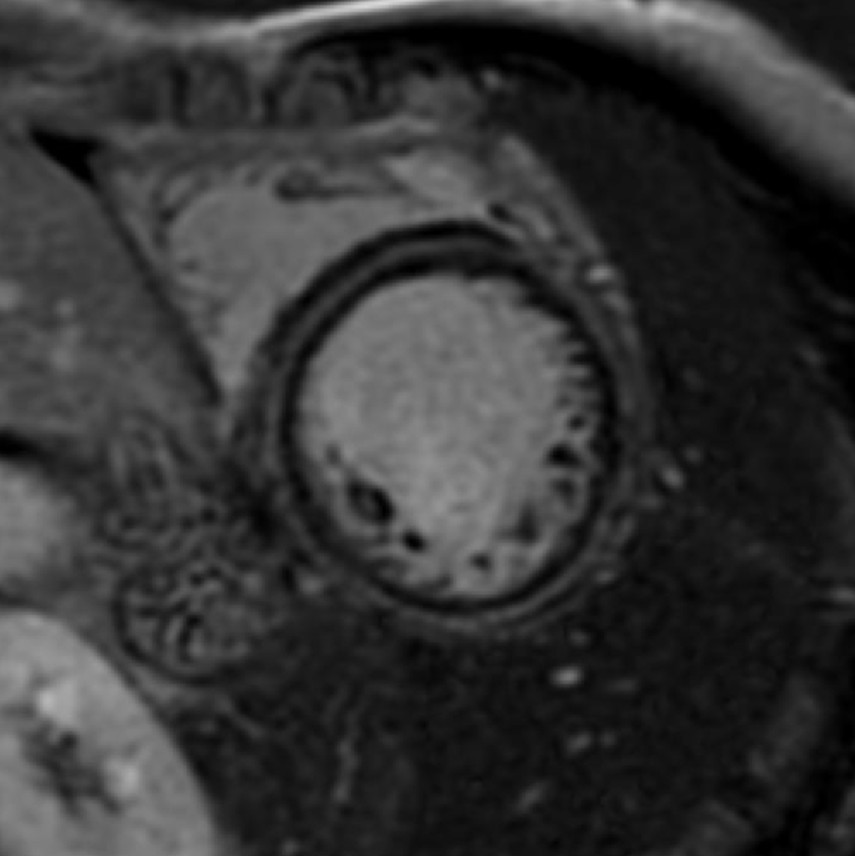
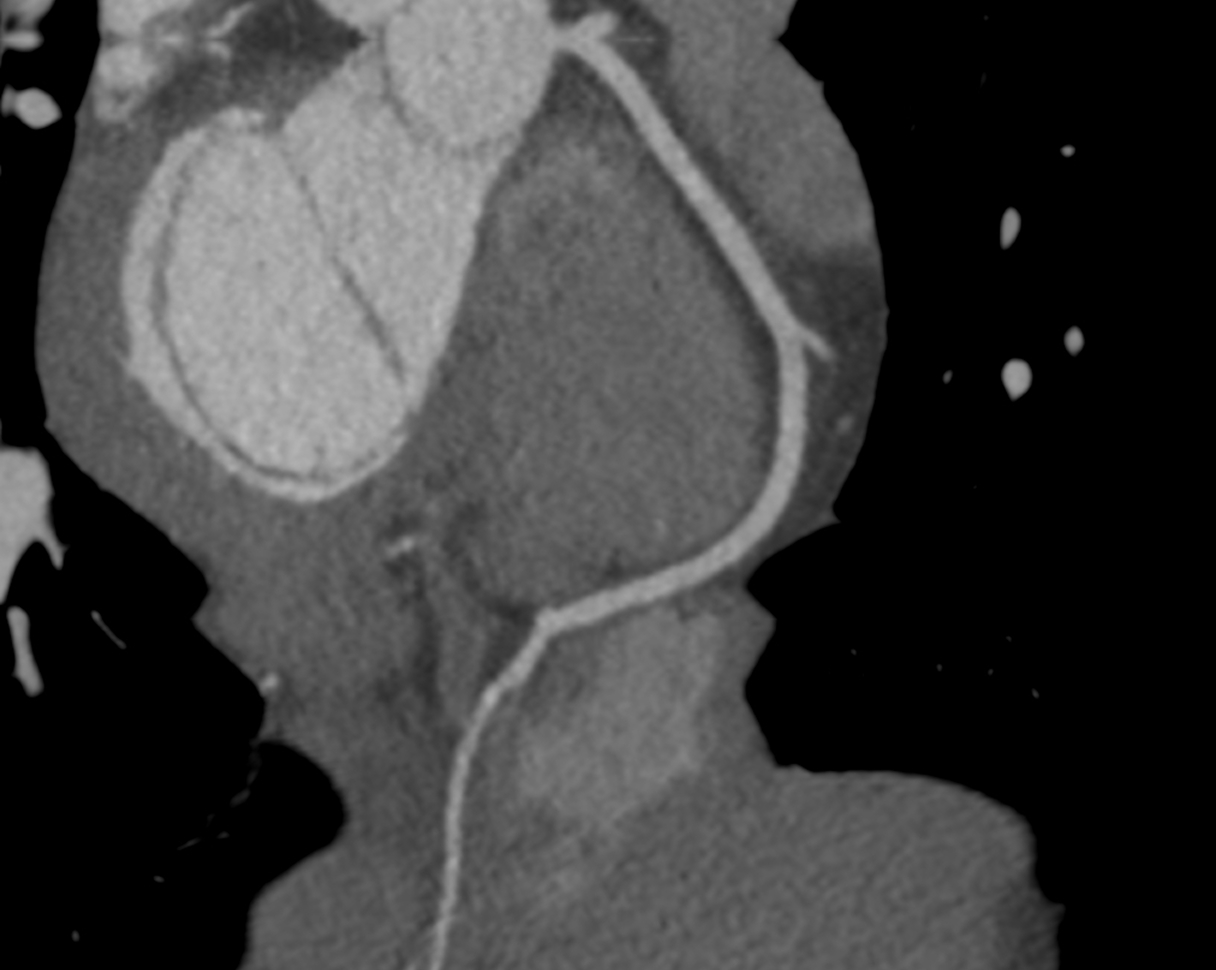
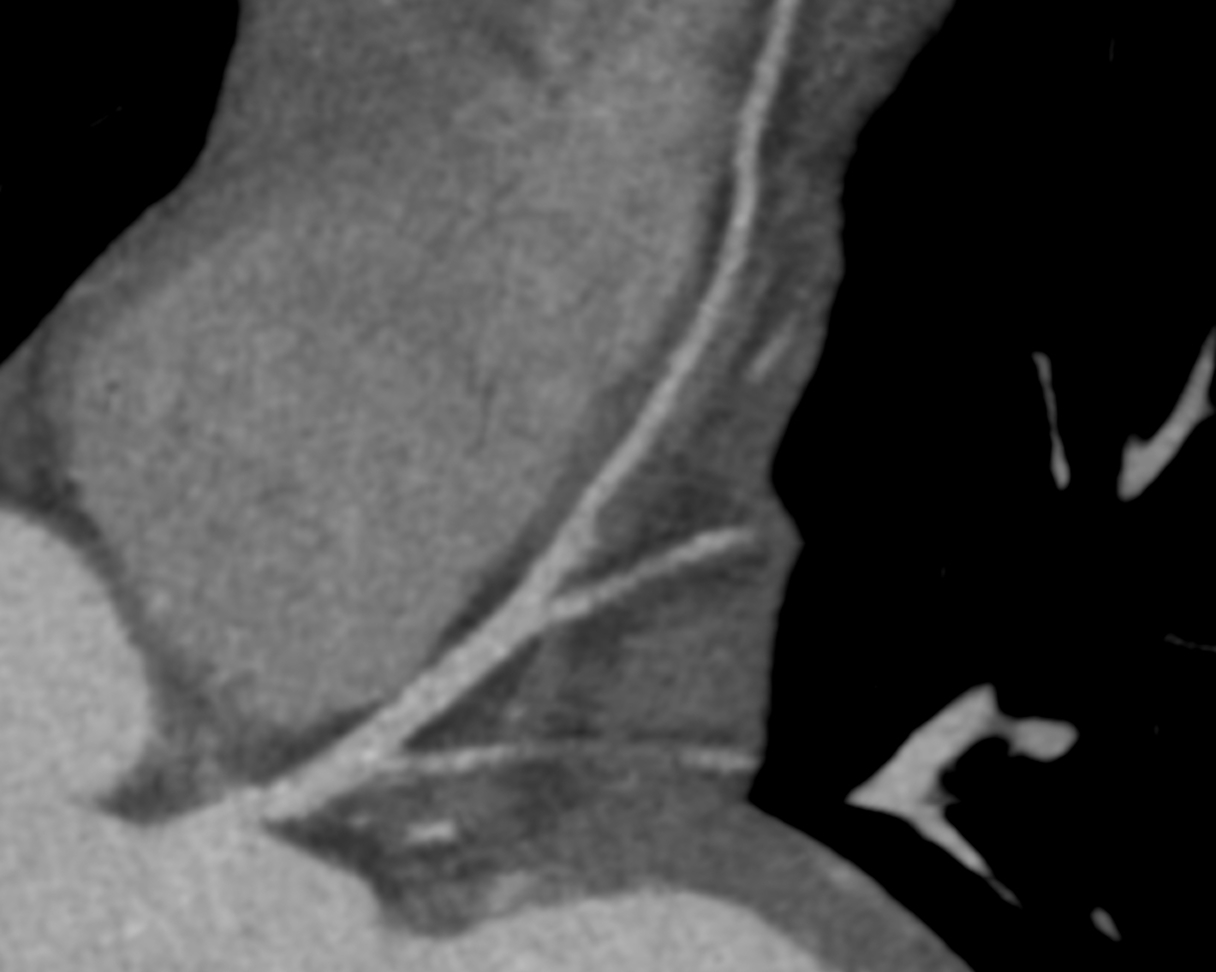
There is a world outside the stent mesh

Saima Mushtaq
Direttore dell'Unità Semplice di TC Cardiovascolare Centro Cardiologico Monzino IRRCS, Milano
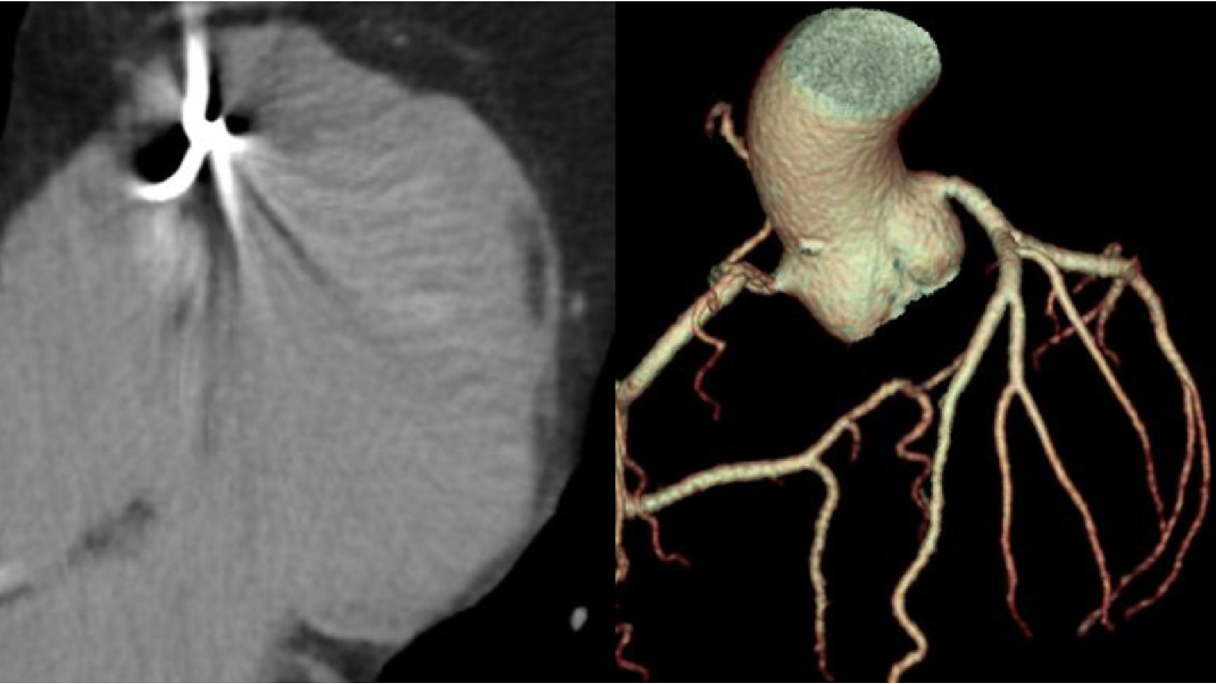
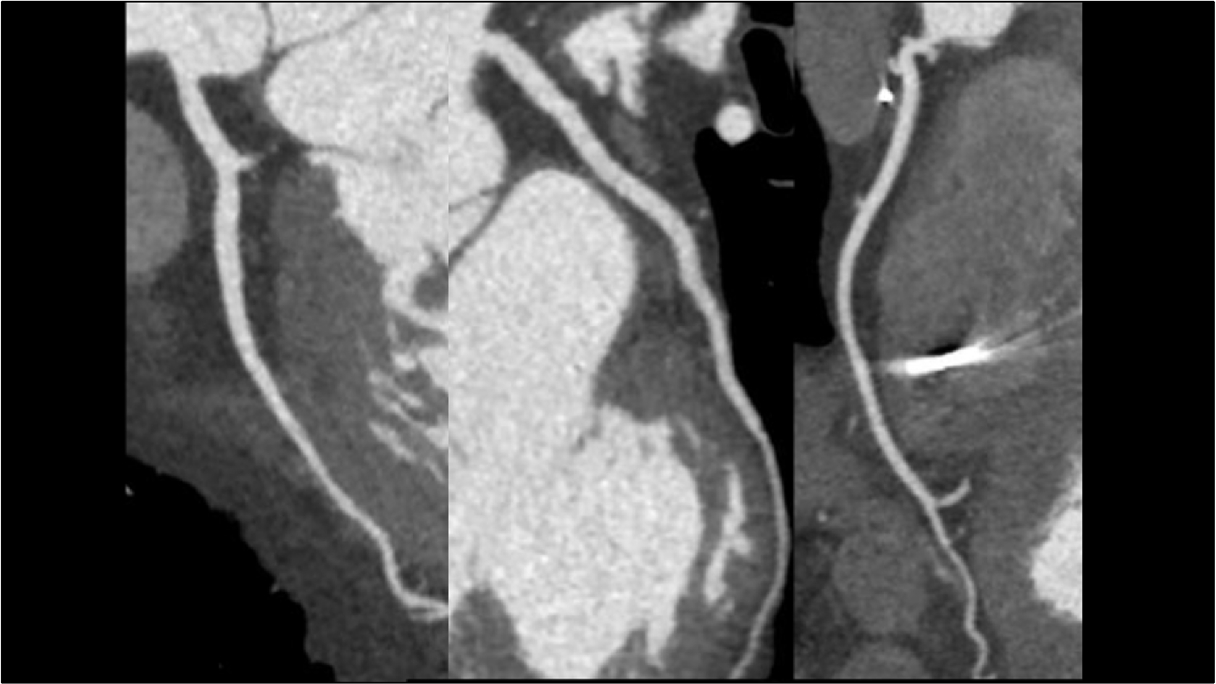
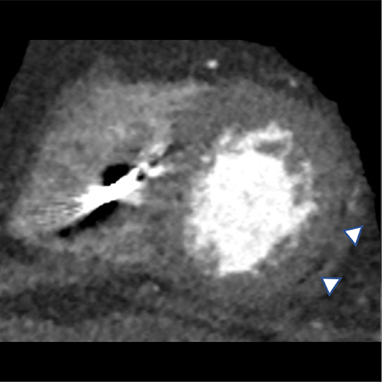
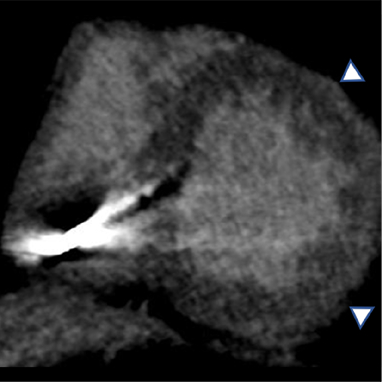
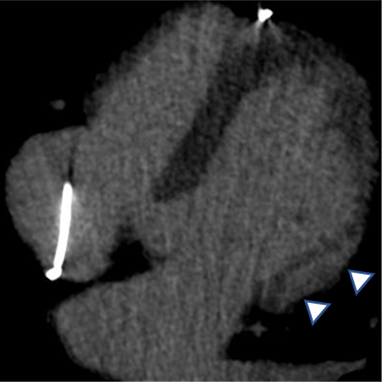
Anamnesi
- Uomo, 52 anni
- Anamnesi di cardiomiopatia dilatativa con disfunzione sistolica moderata del ventricolo sinistro
- Precedente impianto di ICD per prevenzione secondaria a seguito di episodio di pre-sincope associato a tachicardia ventricolare sostenuta (SVT)
- L'ICD ha recentemente erogato una scarica per interrompere un nuovo episodio di tachicardia ventricolare sostenuta.
Aquisizione
- TC del torace senza mezzo di contrasto CCTA con gating 0,23 sec 100 kV, 800 mAs HR: 55 bpm
- Late CCT (5 min post-contrasto): 70 kV, 1300 mAs
- CTDi: 12.7; DLP: 976 mGy/cm
Iniezione
- 50 ml@5 ml/sec + 50 ml di fisiologica @4 ml/sec per CCTA
- 70 ml@3 ml/sec + 30 ml di fisiologica subito dopo CCTA per Late Enhancement
Gestione dati cardiaci
Aquisizione in console CCTA- DLIR-H 0.625 mm
- 0-100% R-R
- DLIR-H 0.625 mm
- 75% R-R
- Smart phase SSF2 vasi coronarici
- MPR in average mode@8 mm per Late
- Ricostruzione polmonare
Beneficio clinico
Nei pazienti con tachicardia ventricolare (VT), la risonanza magnetica cardiaca è spesso limitata dalla presenza di dispositivi impiantabili, che possono generare artefatti significativi vicino allo stimolatore, e dalle condizioni clinico-emodinamiche, potenzialmente instabili, che richiedono un monitoraggio continuo.
I recenti progressi nella tomografia computerizzata cardiaca (TC cardiaca) hanno consolidato questa tecnica come una modalità di imaging completa, che offre una valutazione anatomica, strutturale e funzionale con una precisione diagnostica comparabile alla RM.
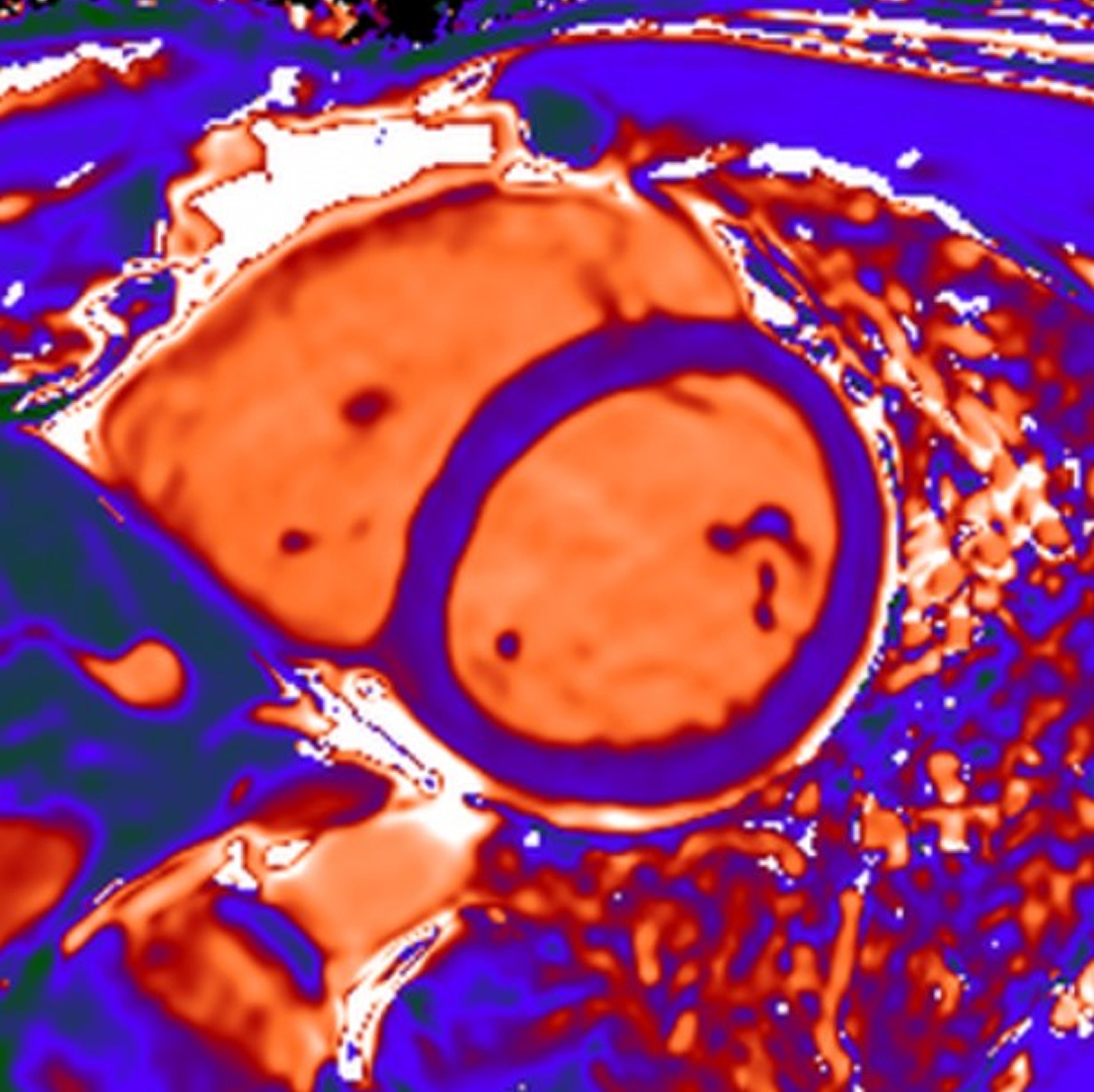
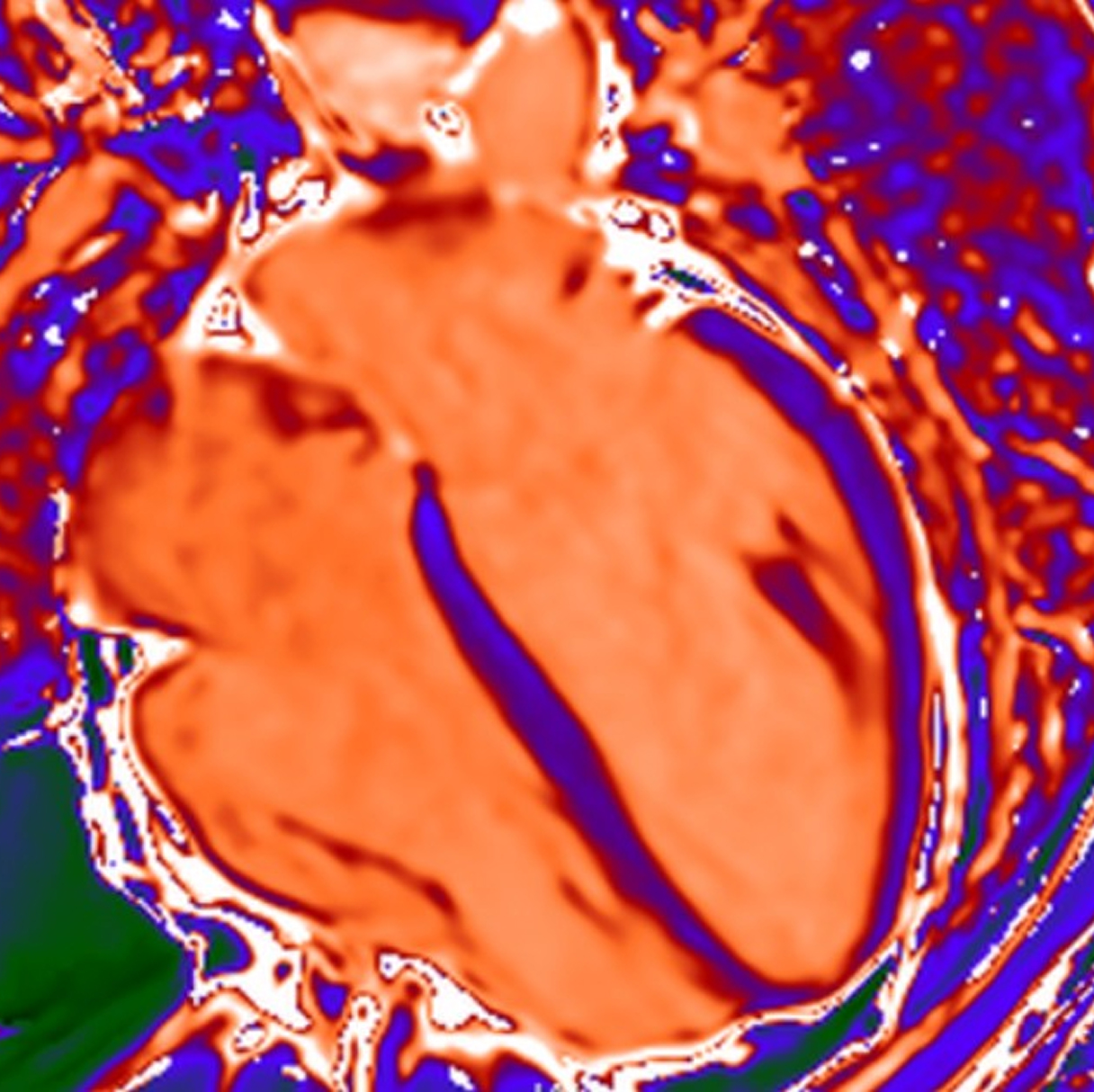
In questo caso, la TC cardiaca ha mostrato l'assenza di malattia aterosclerotica significativa nelle arterie coronarie epicardiche e ha permesso una caratterizzazione dettagliata del substrato aritmogeno, identificando l'infiltrazione adiposa della parete laterale del ventricolo sinistro, a livello medio-apicale, associata a un ampio potenziamento tardivo subepicardico in un pattern “ad anello”.
Questi risultati sono stati determinanti nel guidare la mappatura elettroanatomica e la pianificazione procedurale, consentendo l'integrazione della visualizzazione della cicatrice miocardica con strutture.
Vuoi approfondire il caso con un nostro esperto?
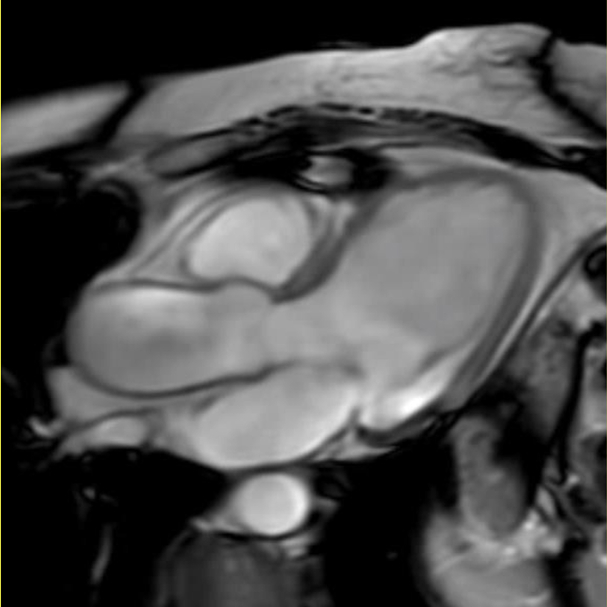
Imaging Cardiaco
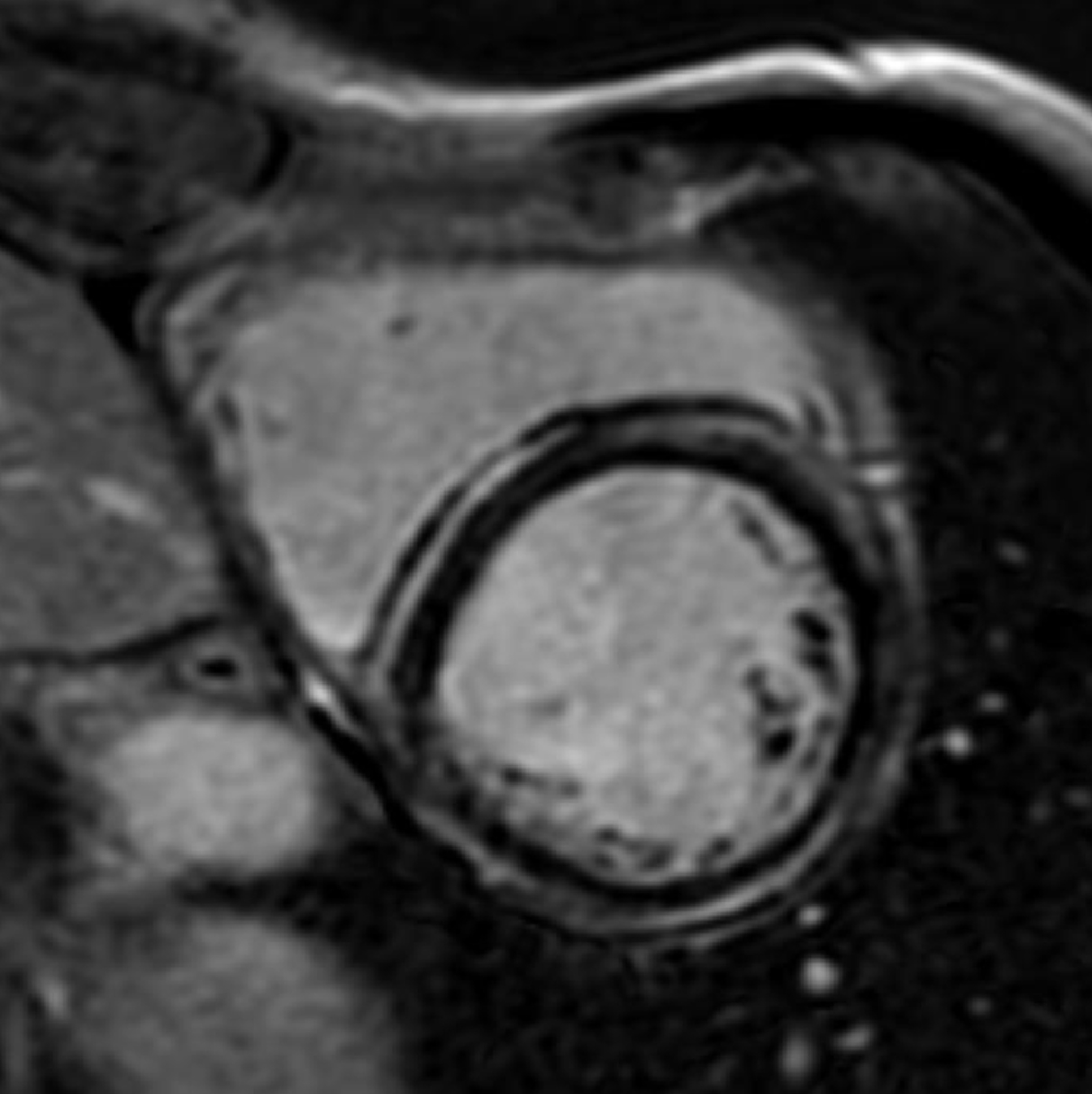
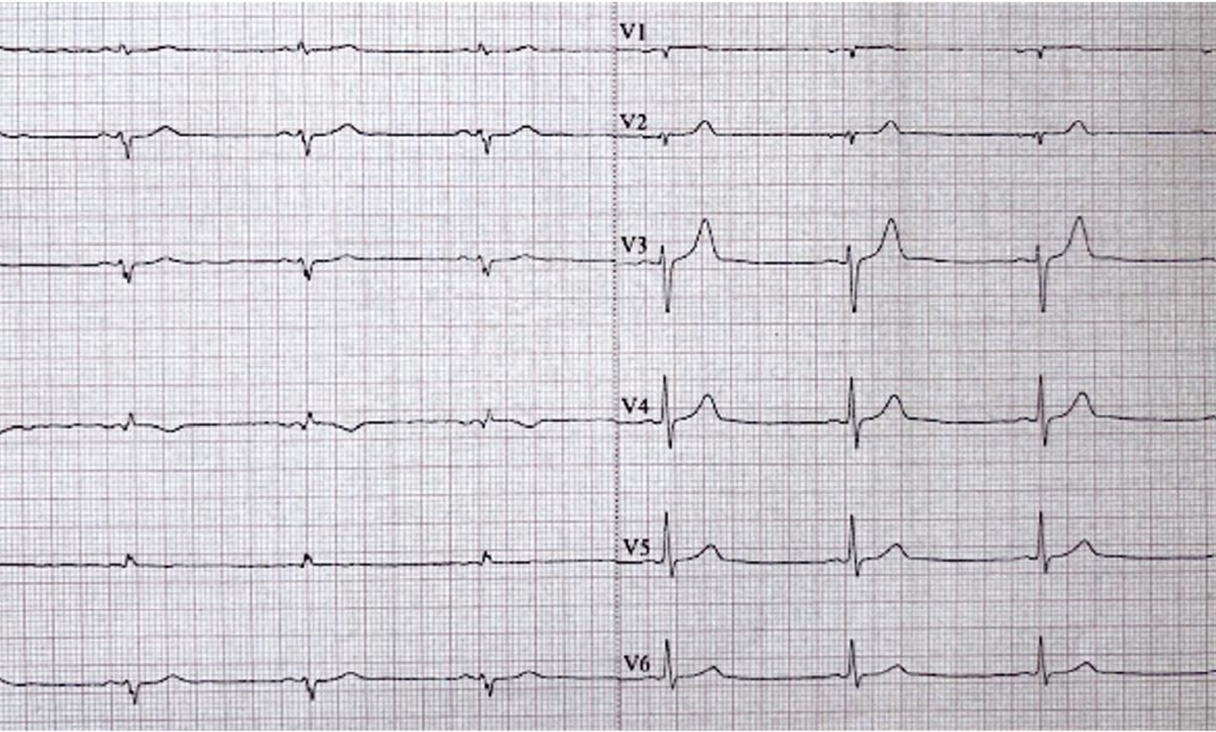
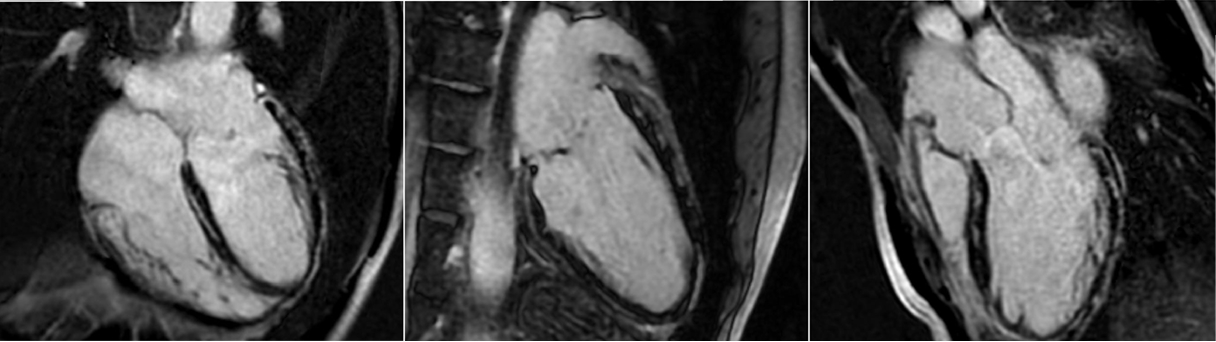
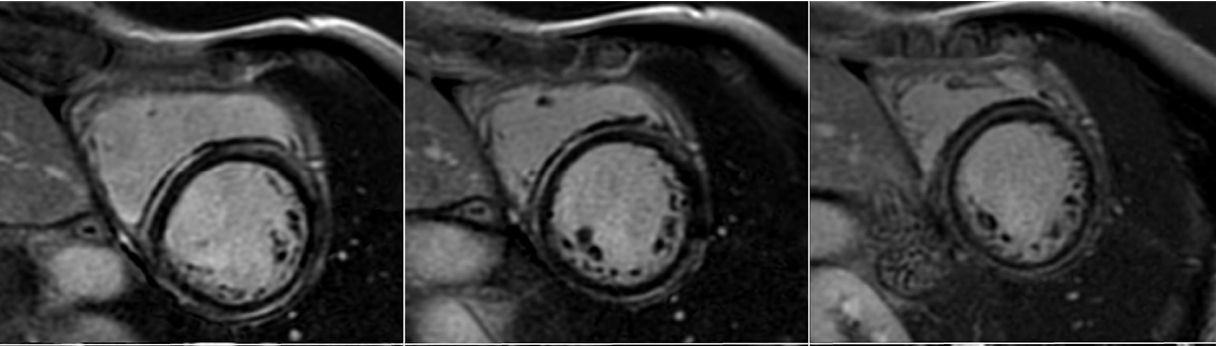
Fifty shades of grey

Marcello De Santis
Medico Radiologo presso Diagnostica per Immagini, IRCCS San Raffaele, Roma
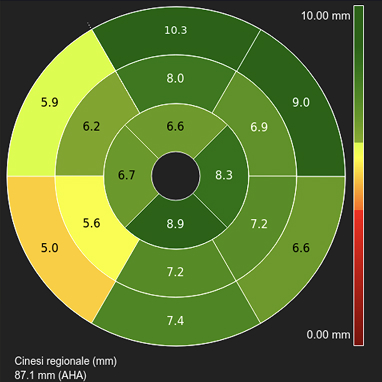 Bull's eye
con valori T2
Bull's eye
con valori T2
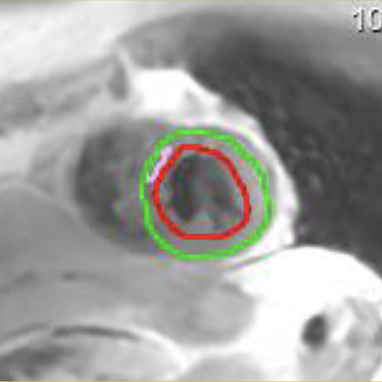 SA Contours
T2 Map
SA Contours
T2 Map
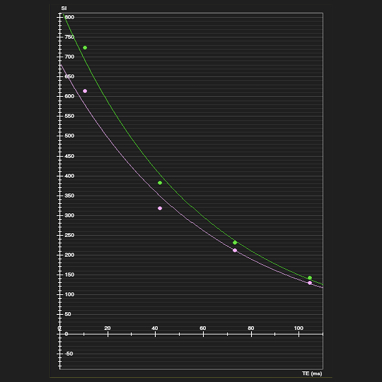 Curve di
rilassamento T2
Curve di
rilassamento T2
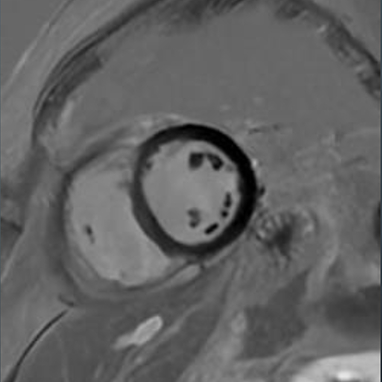 SA LGE
mid
SA LGE
mid
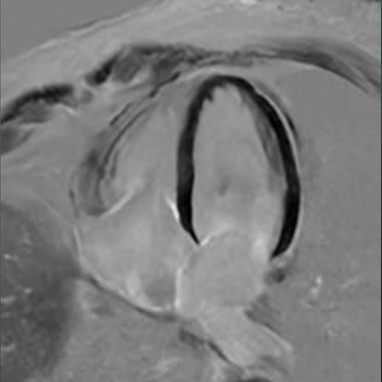 HLA
HLA
Anamnesi
- Donna di 55 anni, con recente MINOCA
Aquisizione
- SSFP cine FIESTA con Sonic DL™ DL™ (6 RR), T2 mapping e imaging MDE bright-blood con tecnica PSIR
Reperti di imaging
- Ipochinèsia lieve del setto medio del ventricolo sinistro (LV)
- Lieve aumento del tempo di rilassamento T2 allo stesso livello (61 msec)
- Nessuna anomalia all’imaging MDE bright-blood PSIR
- Presenza di lieve enhancement tardivo transmurale (LGE) nel setto medio del LV all’imaging MDE dark- blood PSIR
Diagnosi
Sindrome di Takotsubo in fase subacuta, variante medio-ventricolare.
Vuoi approfondire il caso con un nostro esperto?
Imaging Cardiaco
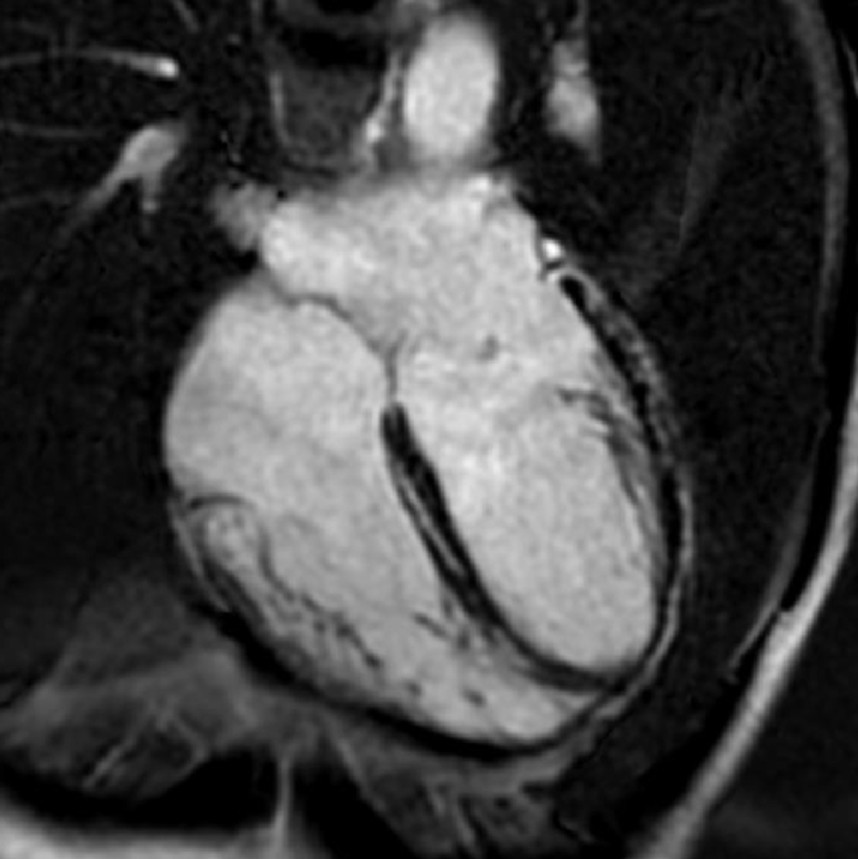
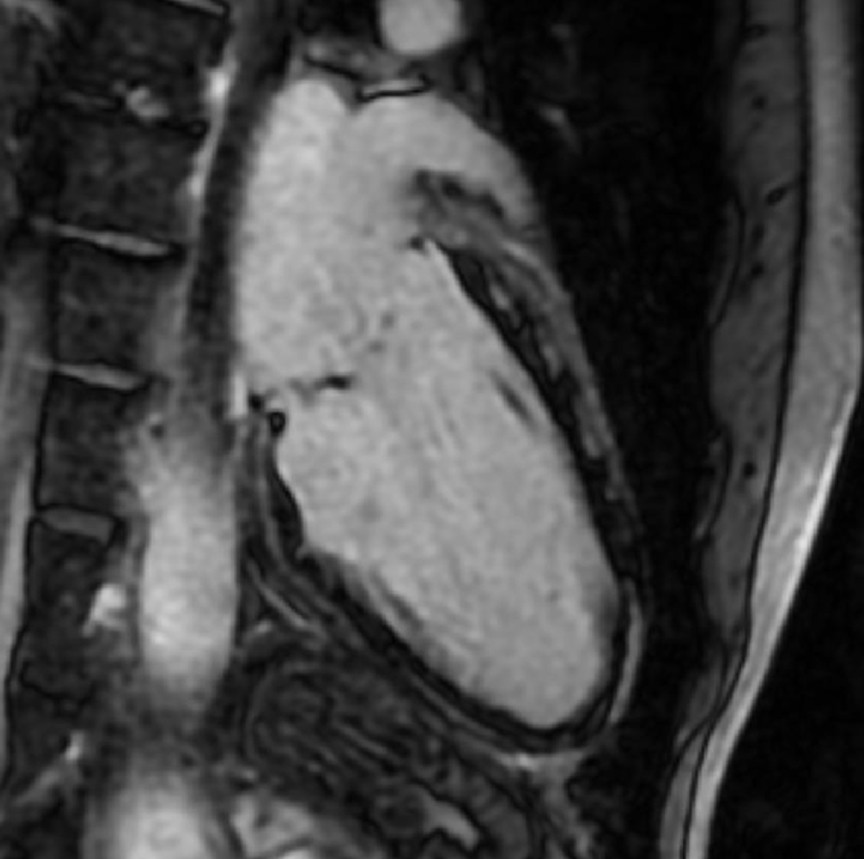
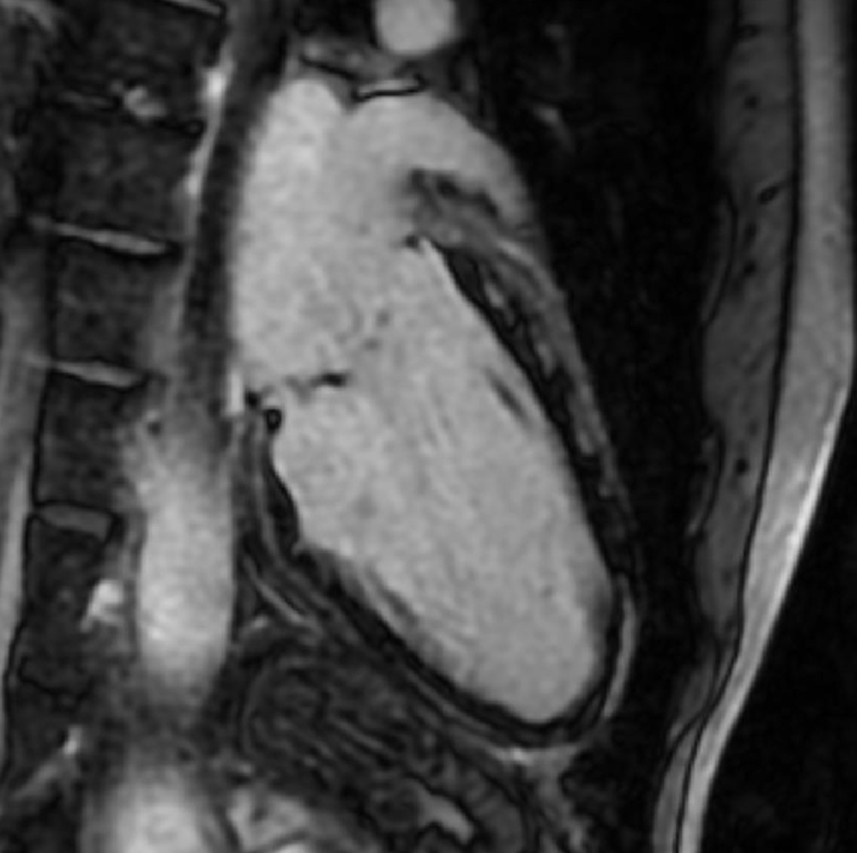
The great mimicker

Marcello De Santis
Medico Radiologo presso Diagnostica per Immagini, IRCCS San Raffaele, Roma
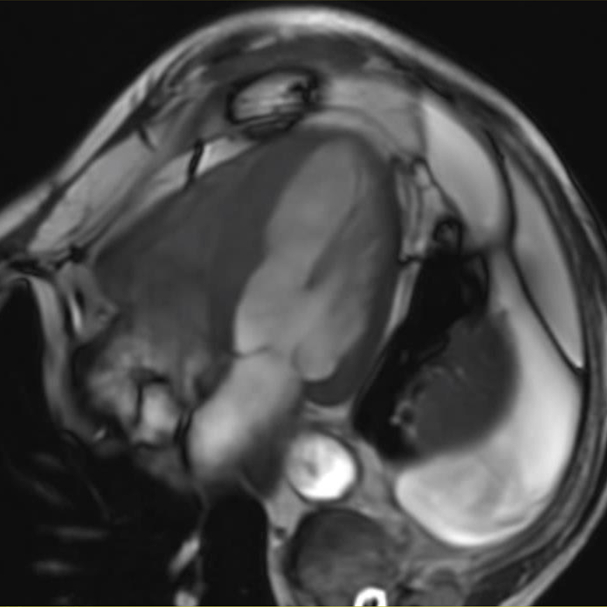
 SA
TIR T2
SA
TIR T2
Anamnesi
- Uomo di 75 anni, con cardiopatia ischemica cronica (CAD), recentemente sottoposto a intervento di bypass aorto-coronarico. Consolidazione del lobo inferiore sinistro con versamento pleurico, non responsiva alla terapia antibiotica. Insorgenza recente di aritmie ventricolari complesse (ectopie multifocali e NSVT)
Indicazioni per CMR
- Aritmie ventricolari correlate a CAD (IMA acuto? Peggioramento dello scompenso cardiaco?)
Acquisizione
- Imaging cine SSFP FIESTA sugli assi lungo e corto con Sonic DL™ (3 RR)
- Sequenza STIR su asse corto in respiro libero e imaging MDE PSIR su asse corto
Reperti di imaging
- Edema a chiazze di aspetto simil massivo al punto di inserzione posteriore basale del ventricolo destro (RV), con localizzazione subepicardica. Foci multipli di LGE con evidenza del "triangle sign" al punto di inserzione posteriore basale del RV, caratterizzati da un'intensità di segnale molto elevata rispetto all’LGE correlato all’infarto (parete laterale del ventricolo sinistro - LV)
Diagnosi
Sarcoidosi cardiaca con coinvolgimento ventricolare sinistro e destro (LV-RV) + consolidazione polmonare atipica + SAPE (versamento pleurico associato a sarcoidosi).
Vuoi approfondire il caso con un nostro esperto?
Imaging Cardiaco
Problemi di microcircolo in un paziente con stent

Gianluca Pontone
Direttore Dipartimento Cardiologia peri-operatoria e Imaging cardiovascolare Centro Cardiologico Monzino IRRCS, Milano

Saima Mushtaq
Direttore dell'Unità Semplice di TC Cardiovascolare Centro Cardiologico Monzino IRRCS, Milano
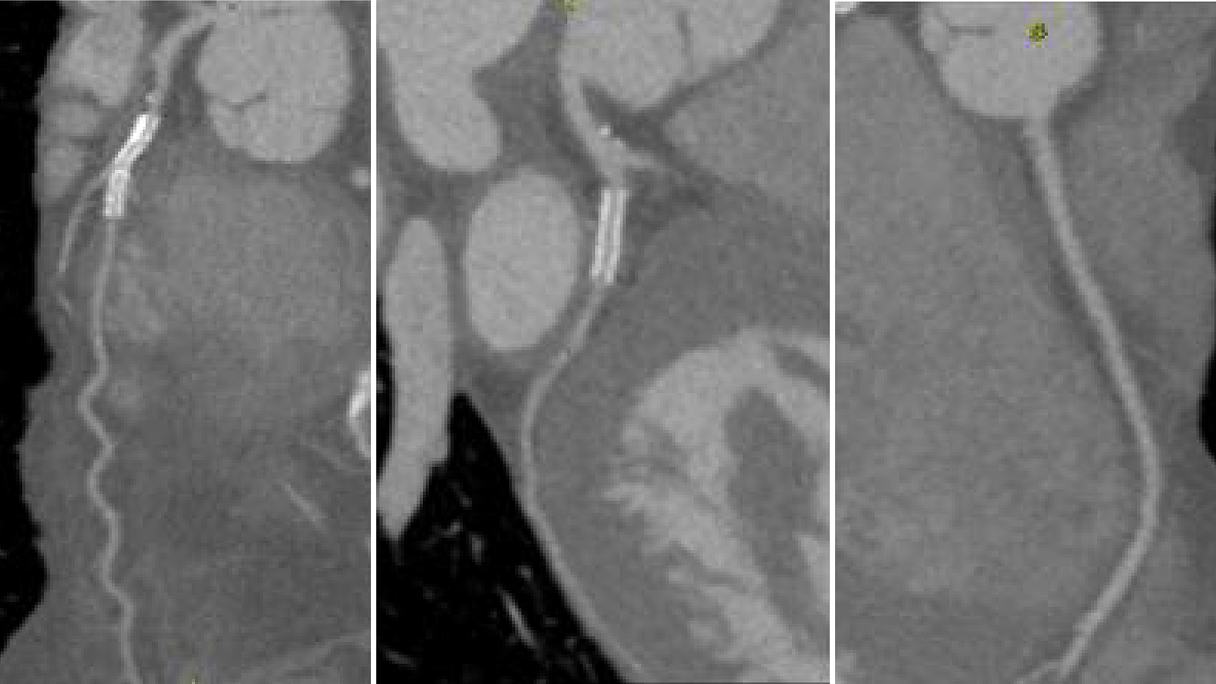 Pervietà
degli stent su LAD, LCX e assenza di stenosi sulla RCA
Pervietà
degli stent su LAD, LCX e assenza di stenosi sulla RCA
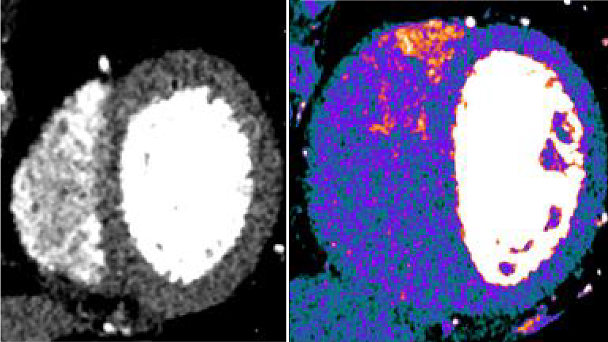 Nessun
difetto di perfusione nella fase a riposo
Nessun
difetto di perfusione nella fase a riposo
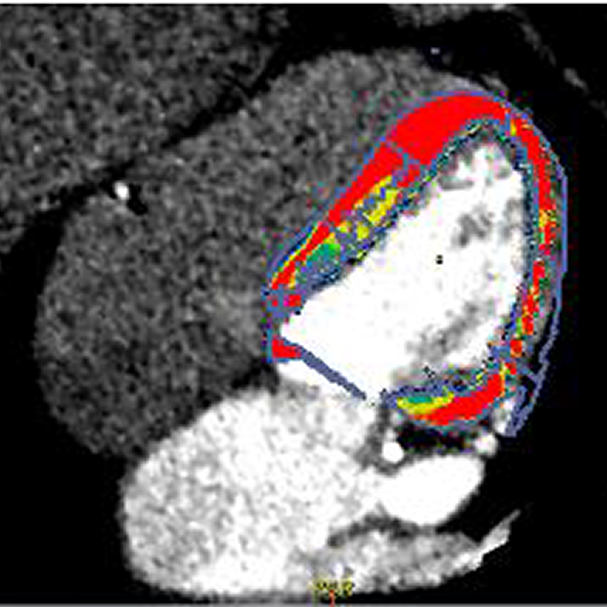
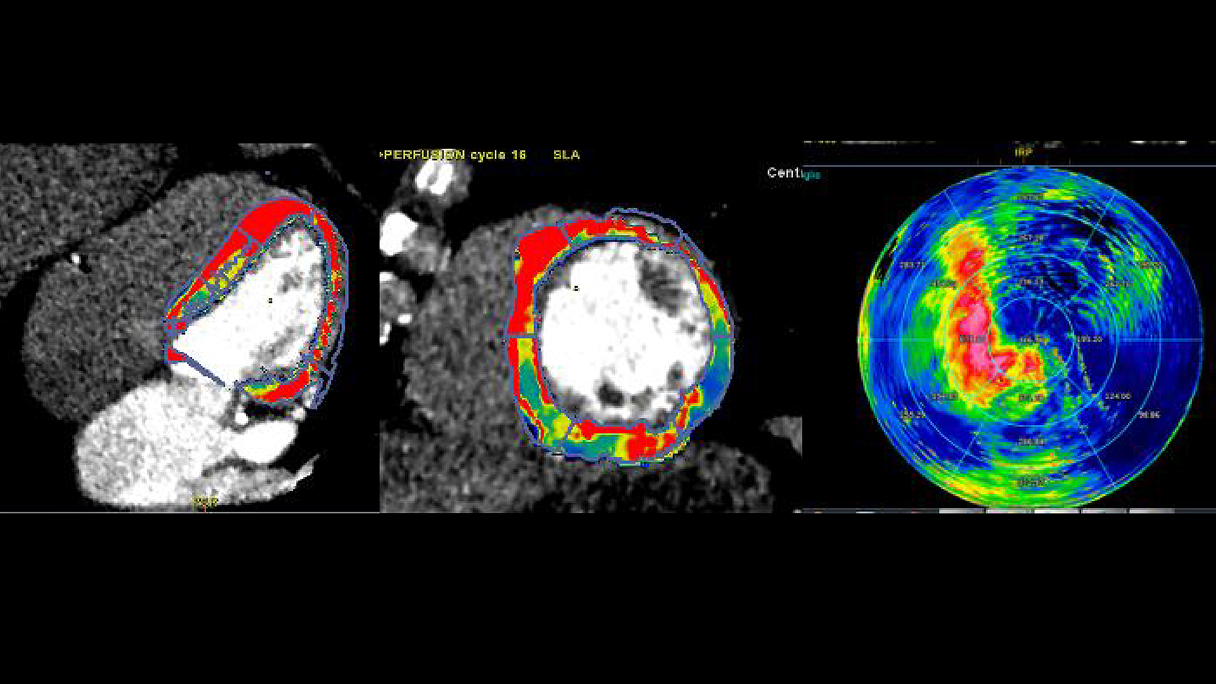 La
perfusione TC dinamica ha mostrato valori patologici di flusso
miocardico (MBF) nel setto e nella parete inferoposterolaterale
La
perfusione TC dinamica ha mostrato valori patologici di flusso
miocardico (MBF) nel setto e nella parete inferoposterolaterale
Anamnesi
- Donna di 65 anni, con ipertensione e storia di coronaropatia (CAD) trattata con stent su LAD, D1 e LCX
- Presenta angina atipica e test da sforzo positivo
Aquisizione
- La paziente è stata sottoposta a Cardio TC con TC di perfusione a riposo
- Dopo 15 minuti, somministrazione di 400 mcg di regadenoson per via endovenosa
- Esecuzione di più scansioni secondo il protocollo dinamico TC
Iniezione
- Iniezione di 50 ml di mezzo di contrasto + 50 ml di soluzione salina a 5 ml/sec
- Durante la fase di stress, somministrazione di 0.7 ml/kg di mezzo di contrasto, seguita da 0.5 ml/kg di soluzione salina a 5 ml/sec
- Mezzo di contrasto con concentrazione di 320 mg/ml
Software di post-elaborazione Console di post-elaborazione
- Registrazione TC dinamica e valutazione del protocollo TC dinamico
Beneficio clinico
Valutazione simultanea non invasiva delle arterie coronarie, della possibile ischemia indotta e dei problemi di microcircolo. L'angiografia coronarica (ICA) ha confermato l'assenza di stenosi significative da restenosi intra-stent (ISR) e stenosi de novo, con un FFR normale e un IMR patologico sulla RCA (IMR 40).
Vuoi approfondire il caso con un nostro esperto?
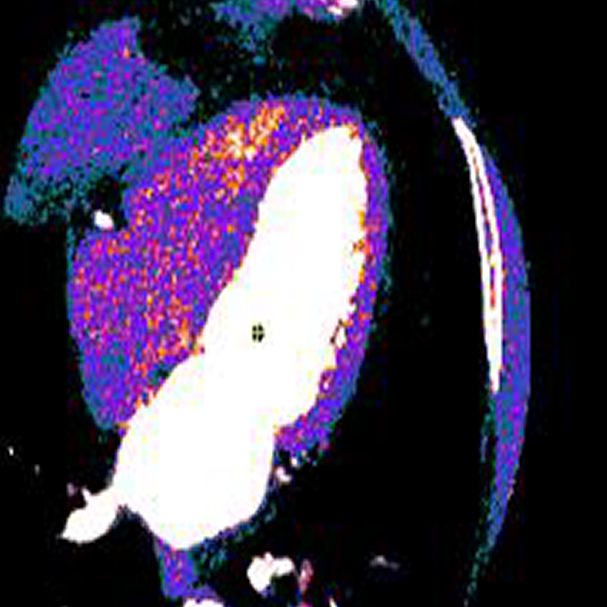
Imaging Cardiaco
Paziente con angina e test da sforzo negativo

Saima Mushtaq
Direttore dell'Unità Semplice di TC Cardiovascolare Centro Cardiologico Monzino IRRCS, Milano

Gianluca Pontone
Direttore Dipartimento Cardiologia peri-operatoria e Imaging cardiovascolare Centro Cardiologico Monzino IRRCS, Milano
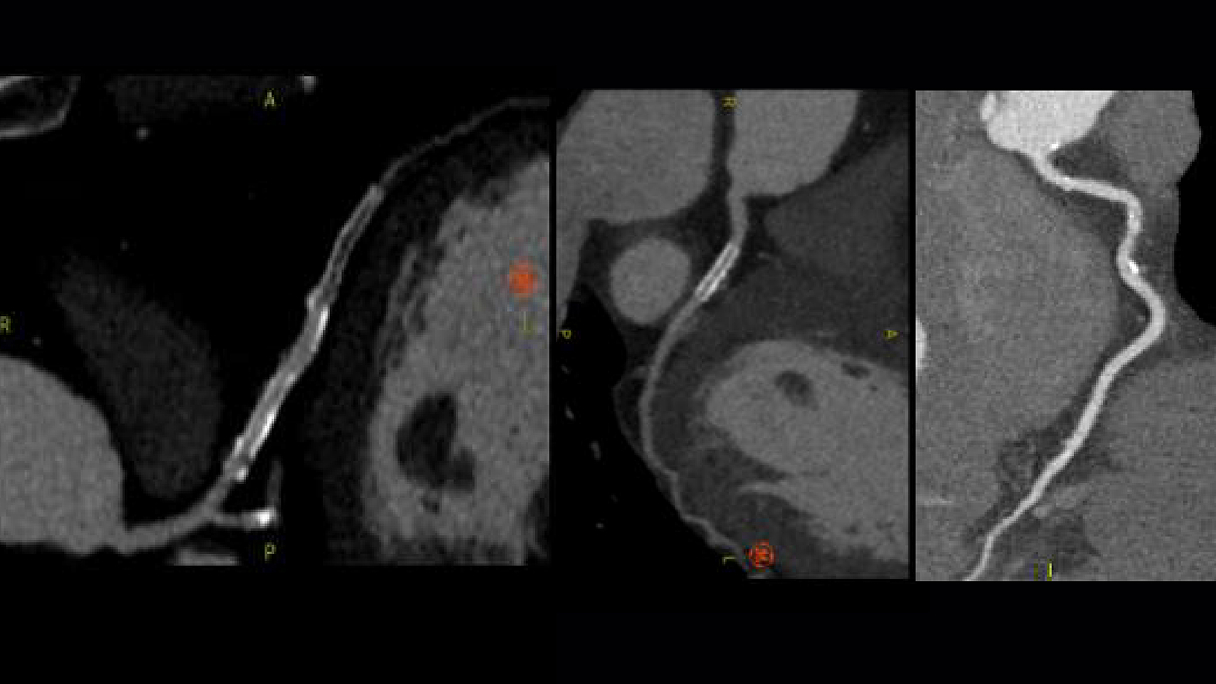 ISR
occlusiva dello stent LAD, pervietà dello stent su LCX, stenosi lieve su
RCA
ISR
occlusiva dello stent LAD, pervietà dello stent su LCX, stenosi lieve su
RCA
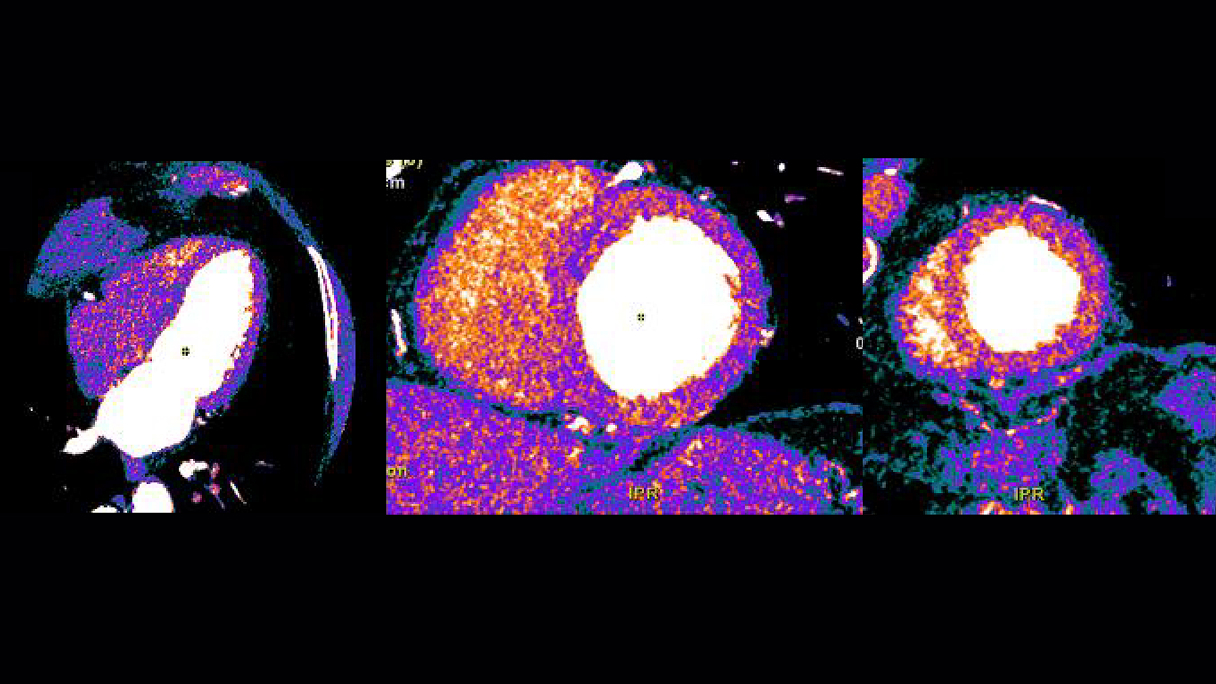 Nessun
difetto di perfusione in fase di riposo
Nessun
difetto di perfusione in fase di riposo
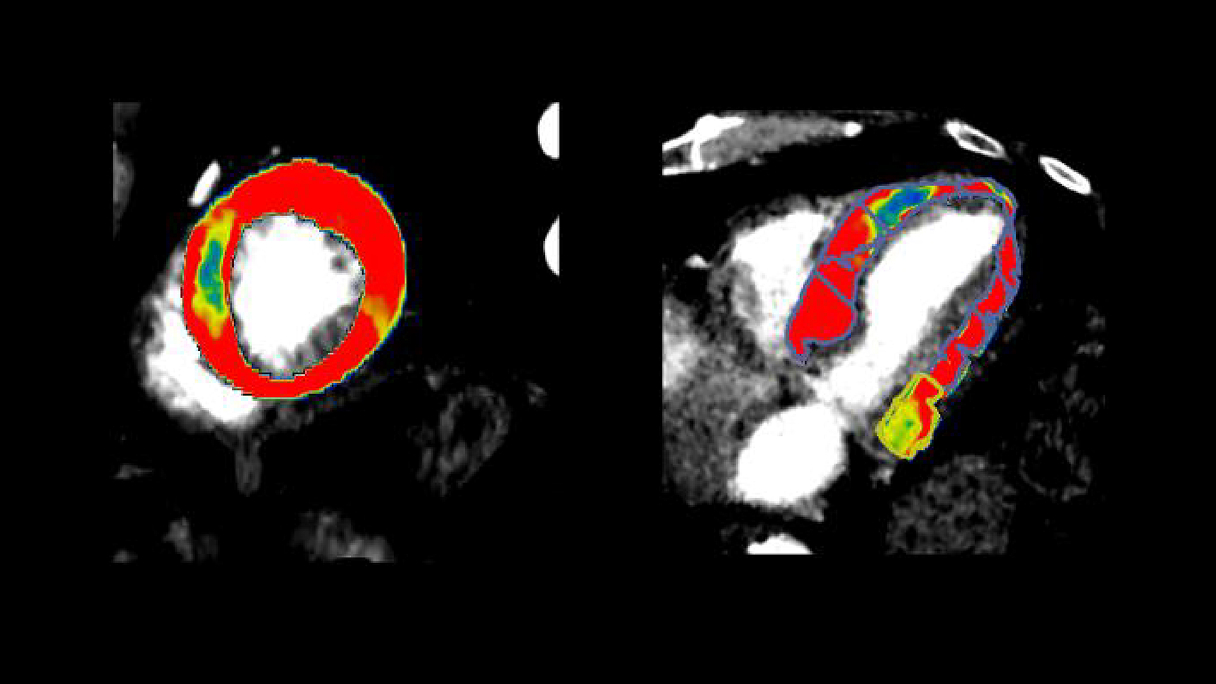 La TC
dinamica di perfusione ha mostrato valori patologici di MBF
nell'anterosetto medio-apicale
La TC
dinamica di perfusione ha mostrato valori patologici di MBF
nell'anterosetto medio-apicale
Anamnesi
- Uomo di 80 anni con ipertensione e storia di CAD con stent su LAD e LCX.
- Angina tipica ma test da sforzo negativo
Aquisizione
- Il paziente è stato sottoposto a TC e TC perfusione a riposo
- A 15 minuti dalla TC precedente, iniezione di 400 mcg di regadenoson intravenoso
- Scansioni multiple secondo il protocollo della TC dinamica
Iniezione
- 50 ml di mezzo di contrasto + 50 ml di soluzione salina a 5 ml/sec.
- 0,7 ml/kg di mezzo di contrasto seguiti da 0,5 ml/kg di soluzione salina a 5 ml/sec per la fase di stress
- Concentrazione del mezzo di contrasto 320 mg/ml
Software di post-elaborazione Console di post-elaborazione
- Registrazione TC dinamica e valutazione del protocollo TC dinamico
Beneficio clinico
Valutazione non invasiva simultanea delle arterie coronarie e dell'ischemia.
Vuoi approfondire il caso con un nostro esperto?

Imaging Cardiaco
Cardiomiopatia ipertrofica
Mutazione MYH7 su base genetica

Azienda ospedaliero-universitaria Sant'Andrea
1.4x1.4x8 mm
00:12 sec BH per slice
Cine1.4x1.4x8 mm
00:11 sec BH
1.4x1.4x8 mm
00:11 sec BH
 T1 Map
T1 Map
1.7x1.7 x8mm
AIR™ Recon DL High
Breathing 3.0x3.0x8 mm3
AIR™ Recon DL High
 Obl
Single Shot Black Blood IR BH
Obl
Single Shot Black Blood IR BH 1.4x1.5x8 mm AIR™ Recon DL High
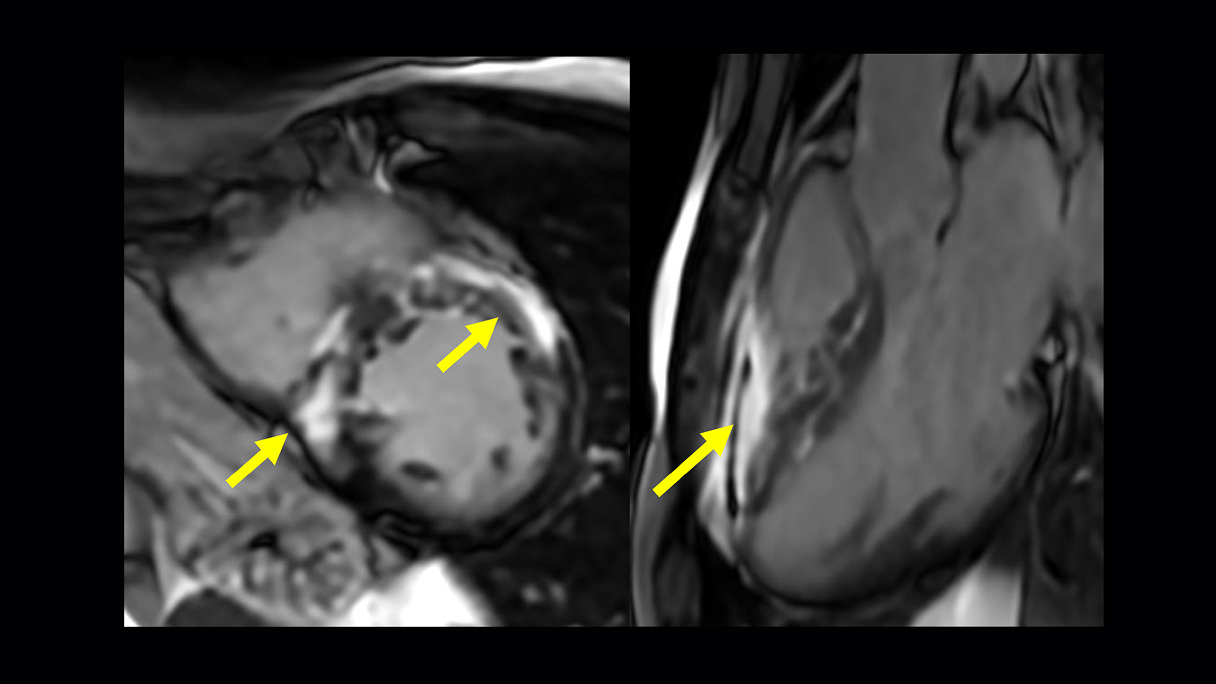 Single
Shot MDE Free Breathing
Single
Shot MDE Free Breathing 1.6x1.6x8 mm AIR™ Recon DL High
1.3x1.3x3 mm TA 1:19 4 slab 12 sec for Slab | AIR™ Recon DL High
Anamnesi
- Paziente di 42 anni con storia di dolore toracico esegue angiografia coronarica e analisi genetica, scopre la mutazione genetica MYH7 correlata alla cardiomiopatia ipertrofica
Beneficio clinico
La mutazione MYH7 è associata alla presenza di due criteri clinici principali: una frazione di accorciamento del ventricolo sinistro (VS) inferiore al 25% e/o una frazione di eiezione del VS inferiore al 45%, con un diametro telediastolico del VS superiore al 117% del valore previsto (corretto per età e superficie corporea secondo la formula di Henry), in assenza di condizioni di carico anomale o di una malattia coronarica tale da giustificare un'alterazione globale della funzione sistolica. La patologia può manifestarsi a qualsiasi età e in entrambi i sessi. Spesso si osserva un aumento marcato della massa ventricolare sinistra, mentre lo spessore parietale rimane nei limiti della norma. Possono essere presenti sintomi di insufficienza cardiaca e aritmie. Altre modalità di presentazione includono il riscontro occasionale di cardiomegalia asintomatica o sintomi legati a disturbi della conduzione e complicanze tromboemboliche. In genere, è presente una storia familiare di cardiomiopatia dilatativa (DCM).
Vuoi approfondire il caso con un nostro esperto?
Imaging Cardiaco
Ecocardiografia transtoracica 4D avanzata per una valutazione accurata della rigurgitazione tricuspidale

Luigi Badano
FESC, FACC, MD, PhD, Direttore dell'Unità di Imaging Cardiovascolare presso Istituto Auxologico Italiano, IRCCS, Ospedale San Luca, Milano
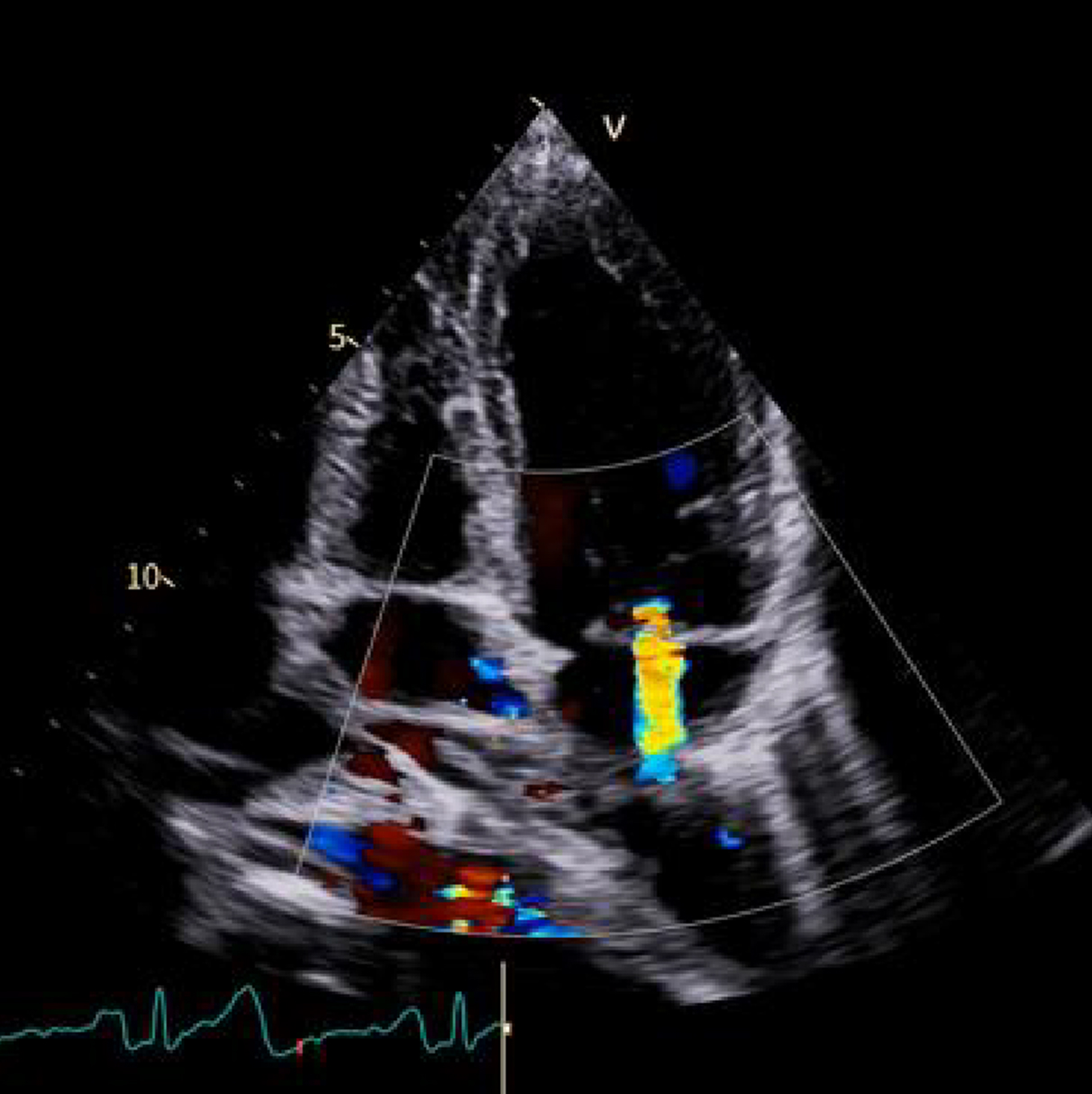
 1. Vista apicale 4CH – Rigurgitazione mitralica
1. Vista apicale 4CH – Rigurgitazione mitralica
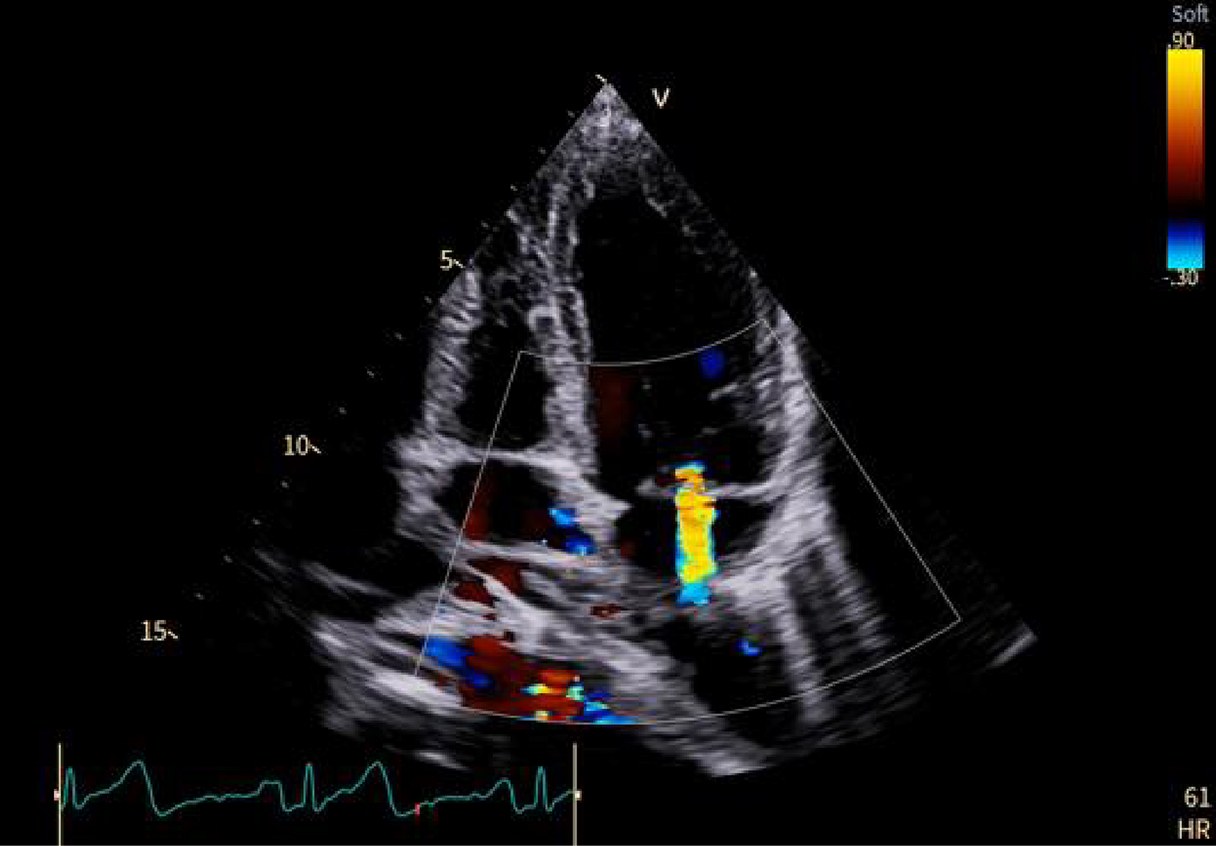
 2. Quantificazione della rigurgitazione mitralica usando il metodo PISA convenzionale
2. Quantificazione della rigurgitazione mitralica usando il metodo PISA convenzionale
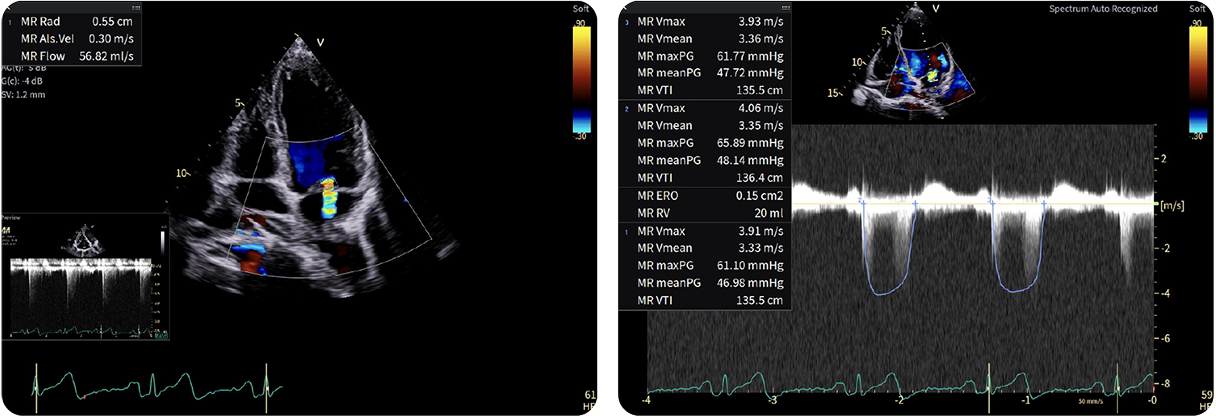
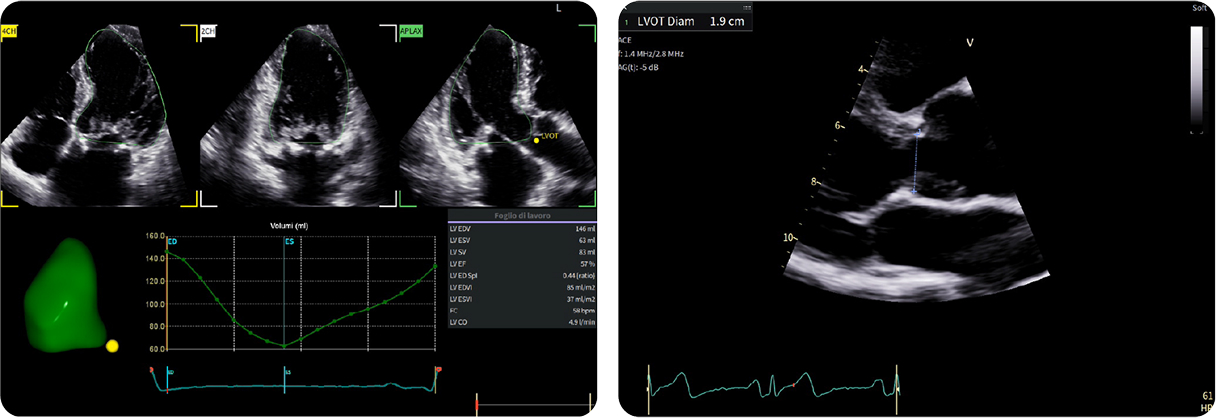 3. Quantificazione della rigurgitazione mitralica 4D con 4D LHQ
3. Quantificazione della rigurgitazione mitralica 4D con 4D LHQUn esame ravvicinato dell’inviluppo del getto rigurgitante rivela componenti protosistoliche e telesistoliche, mentre non si osserva rigurgito durante la mesosistole. In questo caso, il metodo PISA convenzionale probabilmente sovrastima la severità della MR
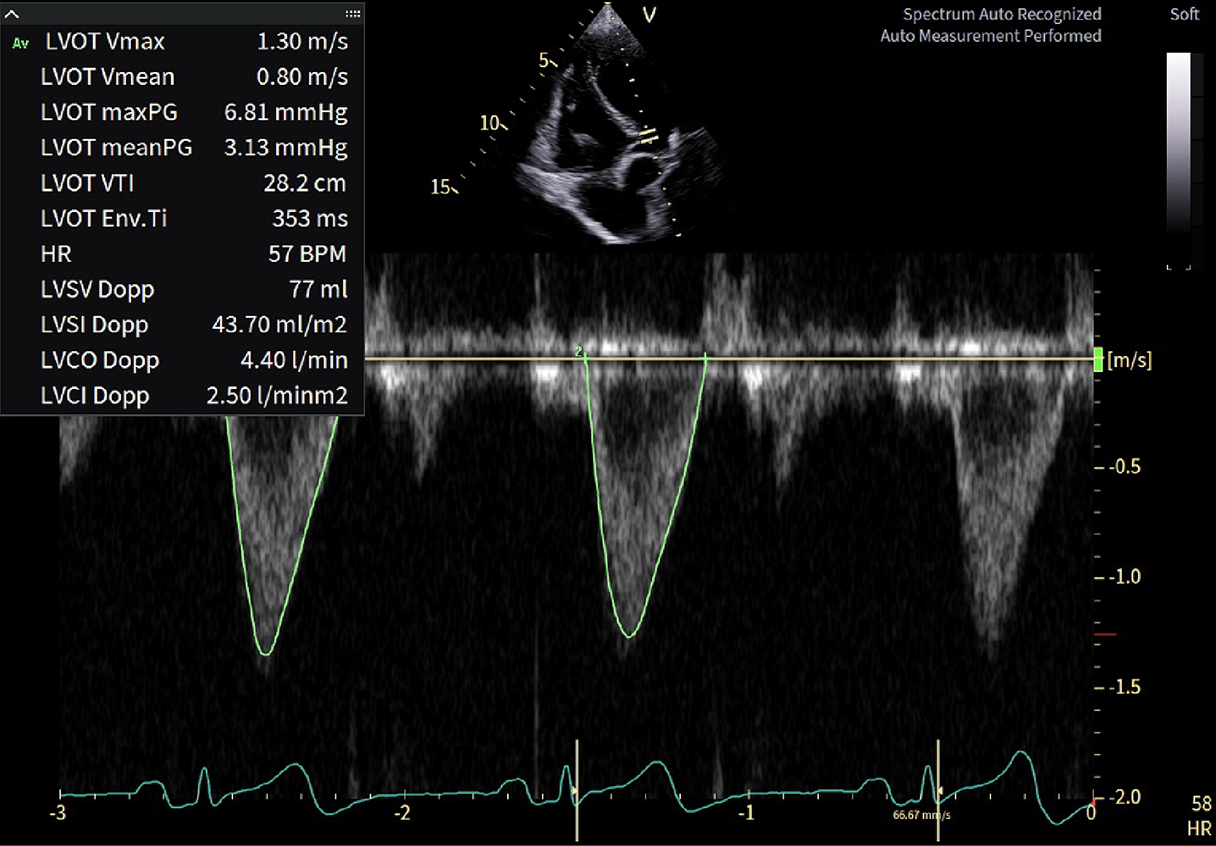 Volume rigurgitante = SVLV − SVLVOT = 83 − 77 = 6 mL. Conferma MR lieve
Volume rigurgitante = SVLV − SVLVOT = 83 − 77 = 6 mL. Conferma MR lieve
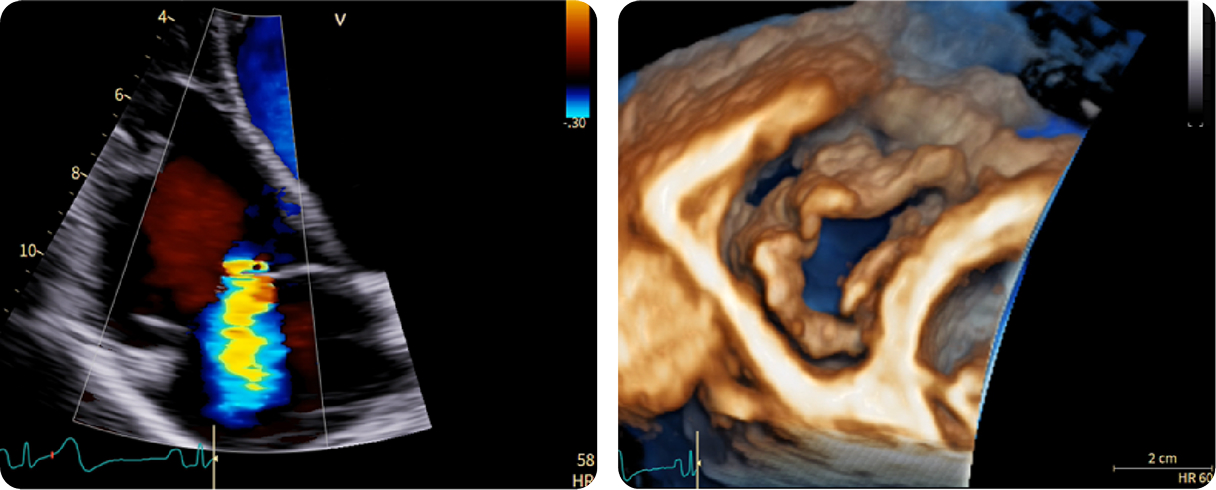 4. Valutazione della funzione e dell’anatomia della valvola tricuspide
4. Valutazione della funzione e dell’anatomia della valvola tricuspideTranstoracica 4D – acquisizione single beat. Immagini anatomiche di alta qualità (sinistra)
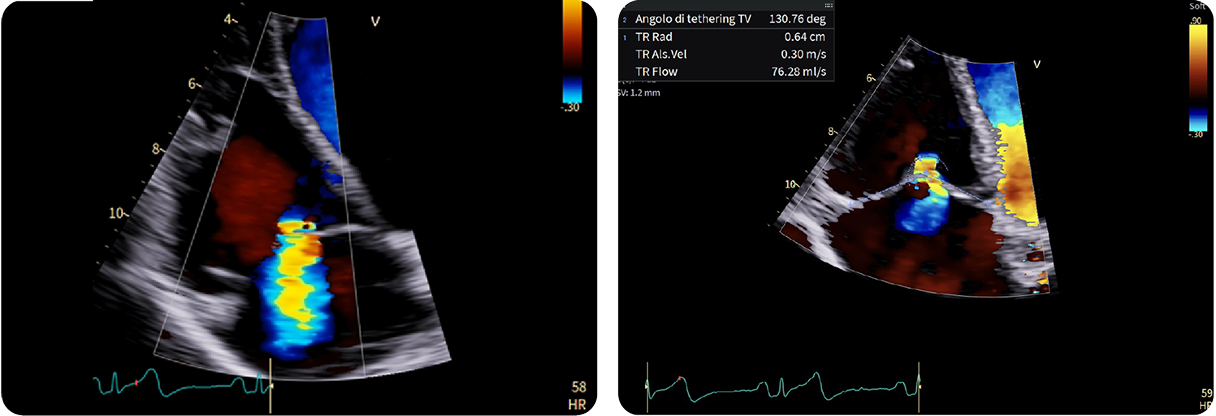 5. Rigurgitazione tricuspidale - Metodo PISA, sfide e considerazioni
5. Rigurgitazione tricuspidale - Metodo PISA, sfide e considerazioniMetodo PISA convenzionale: Volume rigurgitante = 20 mL EROA = 0,33 cm² TR moderata
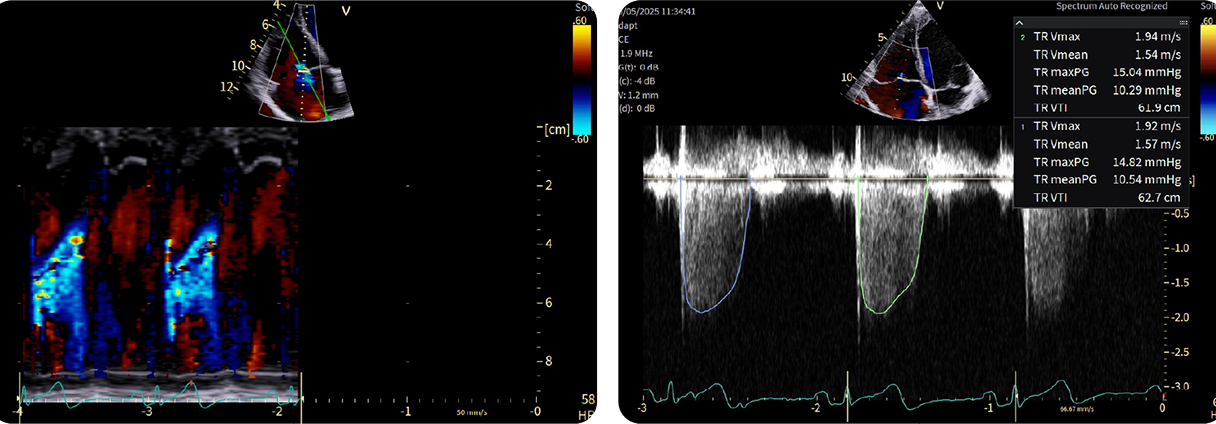 Metodo PISA corretto: Volume rigurgitante = 26 mL EROA = 0,42 cm² TR severa
Metodo PISA corretto: Volume rigurgitante = 26 mL EROA = 0,42 cm² TR severa
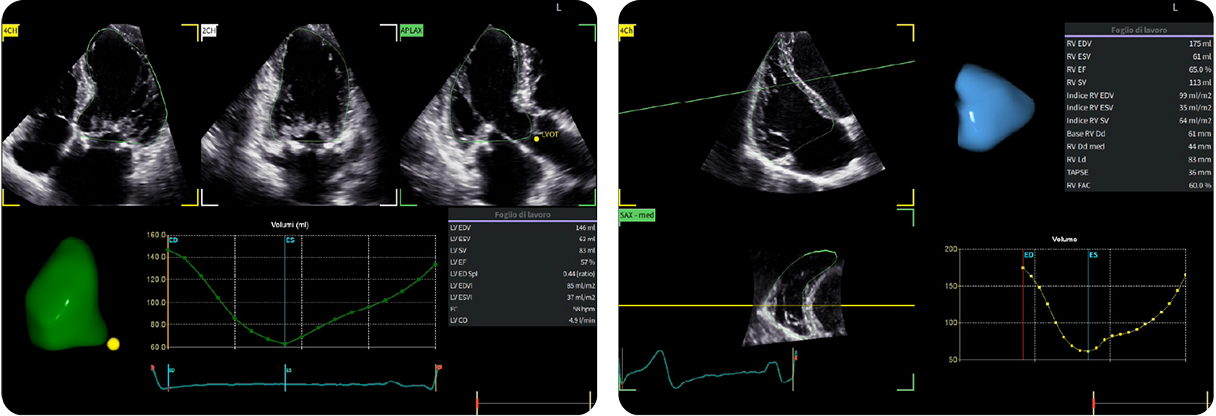 7. Rigurgitazione tricuspidale - metodo volumetrico 4D
7. Rigurgitazione tricuspidale - metodo volumetrico 4DVolume rigurgitante = SVRV - SVLV = 113 - 83 = 30 mL
EROA = Volume rigurgitante/VTITR = 0.48 cm2
Frazione rigurgitante = Volume rigurgitante/SVRV = 27%
Storia clinica del paziente/patologia
- Uomo di 66 anni
- Anamnesi patologica remota negativa. Nessun fattore di rischio cardiovascolare
- Maggio 2025: accesso al Pronto Soccorso per fibrillazione atriale parossistica trattata con amiodarone e.v.
- All'esame obiettivo: soffio sistolico; il paziente viene inviato a ecocardiogramma
Criticità
- Quantificazione di getti rigurgitanti non olosistolici
- Utilizzo del metodo PISA convenzionale per quantificare la rigurgitazione tricuspidale
- Identificazione dell’anatomia della valvola tricuspide e comprensione della fisiopatologia della rigurgitazione tricuspidale
Sistema, sonda e dispositivi utilizzati
- Vivid™ Pioneer
- Sonda 4Vc‑D
- EchoPAC™
Procedura step‑by‑step
- Valutazione della temporalità della MR (olosistolica vs. non olosistolica)
- Valutazione volumetrica 4D della severità della MR
- Metodo PISA corretto per la severità della TR
- Transtoracica 4D per valutare la morfologia della valvola tricuspide
- Apicale RV focus view per il calcolo del volume dell’atrio destro (RA)
- Misurazione 4D dei volumi di LV e RV
- Valutazione volumetrica 4D della severità della TR
- Identificazione della fisiopatologia e classificazione della TR
Conclusioni
L’utilizzo dell’ecocardiografia transtoracica quantitativa 4D e di strumenti dedicati (metodo PISA con correzione dell’angolo e della velocità del jet), nonché di viste specifiche (vista apicale focalizzata sul ventricolo destro per la misurazione del volume dell’atrio destro), ha consentito di determinare correttamente l’eziologia dell'insufficienza tricuspidale (TR) e la sua gravità, al fine di pianificare un follow-up personalizzato e gli obiettivi terapeutici
Imaging follow-up
Ripetere l’ecocardiografia transtoracica 4D a 6 mesi per verificare la progressione della gravità della TR e il rimodellamento delle camere cardiache destre. Trattamento aggressivo per il mantenimento del ritmo sinusale
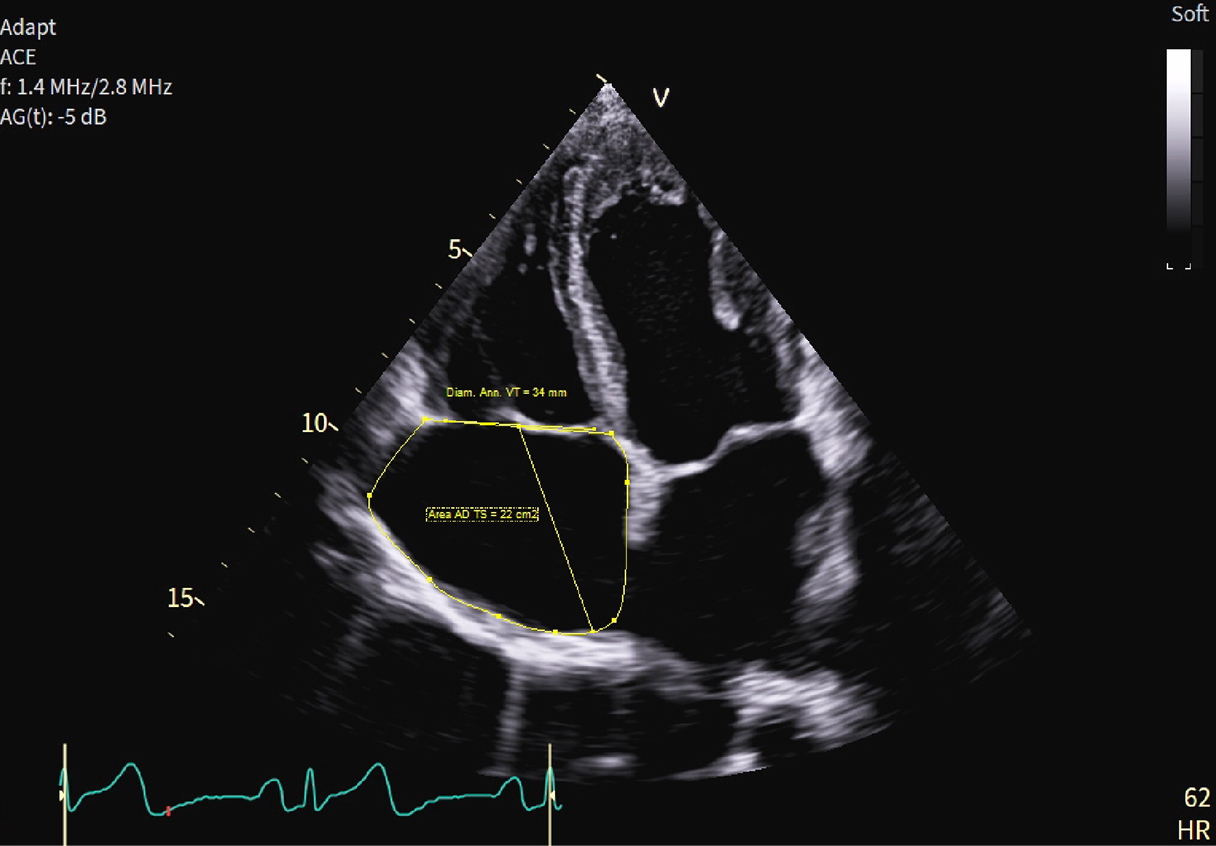 6. Eziologia della rigurgitazione tricuspidale – ecografia raccomandata dalle linee guida
6. Eziologia della rigurgitazione tricuspidale – ecografia raccomandata dalle linee guidaRigurgitazione tricuspidale moderata
Frazione di eiezione del LV normale (57%)
Nessuna cardiopatia sinistra significativa
Atrio sinistro lievemente dilatato = 40 mL/m²
Pressione arteriosa polmonare sistolica = 25 mm Hg
Ventricolo destro lievemente dilatato (area telediastolica = 13,9 cm²)
Funzione del RV normale (FAC = 50%; TAPSE = 2,5 cm)
Atrio destro lievemente dilatato = 40 mL/m²
Rapporto area RA/RV telesistolico aumentato = 1,59
Diametro dell’anulus tricuspide normale = 34 mm
Nessun tenting dei lembi
Conclusione: Sulla base dei parametri verdi, i reperti sono coerenti con rigurgitazione tricuspidale secondaria atriale. Tuttavia, il diametro normale dell’anulus tricuspide è in contrasto con questa diagnosi
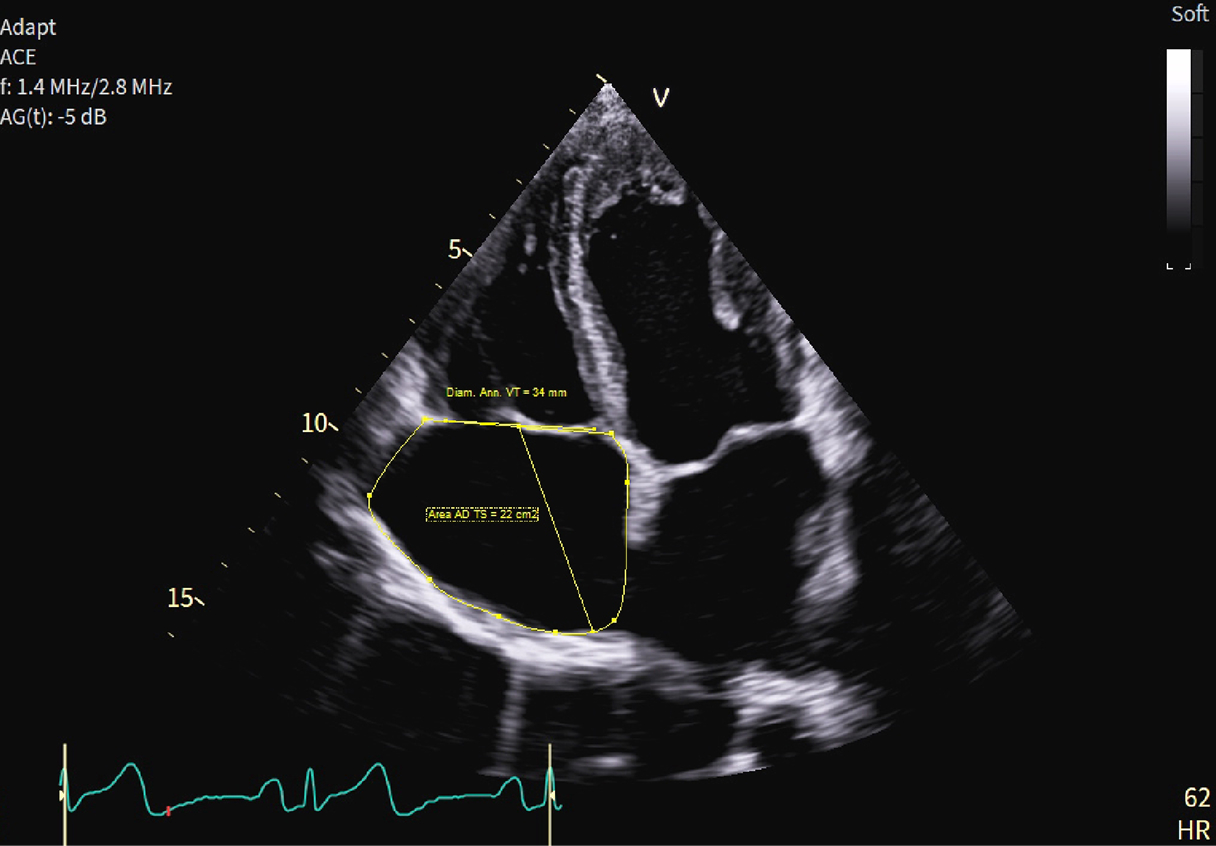 8. Eziologia della rigurgitazione tricuspidale
8. Eziologia della rigurgitazione tricuspidale
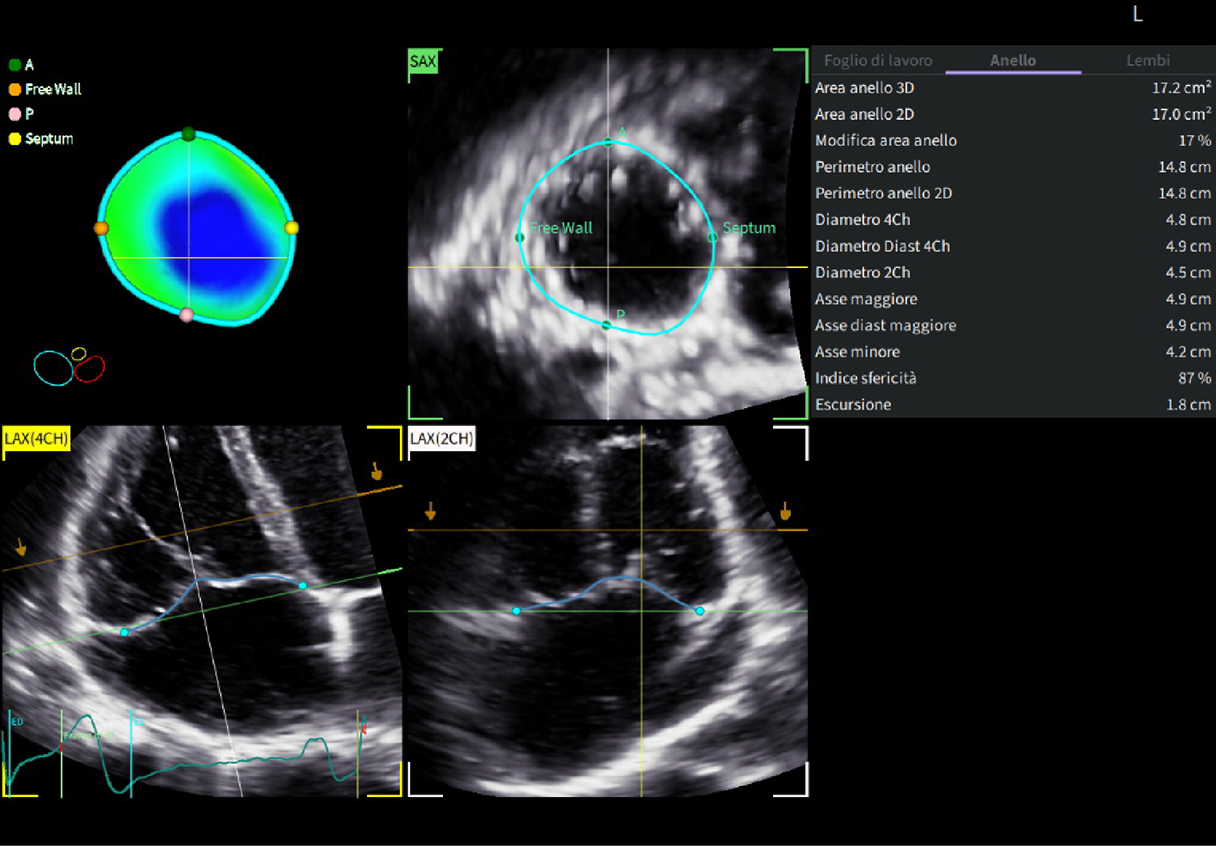 Conclusione: Utilizzando un dataset 4D e misurando l’anulus tricuspide con Auto TVQ,
si ottiene la misura reale dell’anulus. Ora tutti i parametri sono coerenti con la diagnosi: la TR secondaria atriale può essere confermata con fermezza
Conclusione: Utilizzando un dataset 4D e misurando l’anulus tricuspide con Auto TVQ,
si ottiene la misura reale dell’anulus. Ora tutti i parametri sono coerenti con la diagnosi: la TR secondaria atriale può essere confermata con fermezza
Vuoi approfondire il caso con un nostro esperto?
Imaging Cardiaco
Avanzamenti nell'imaging della Cardiomiopatia Ipertrofica

Denisa Muraru
FESC, FACC, MD, PhD, Istituto Auxologico Italiano, IRCCS, Ospedale San Luca, Milano
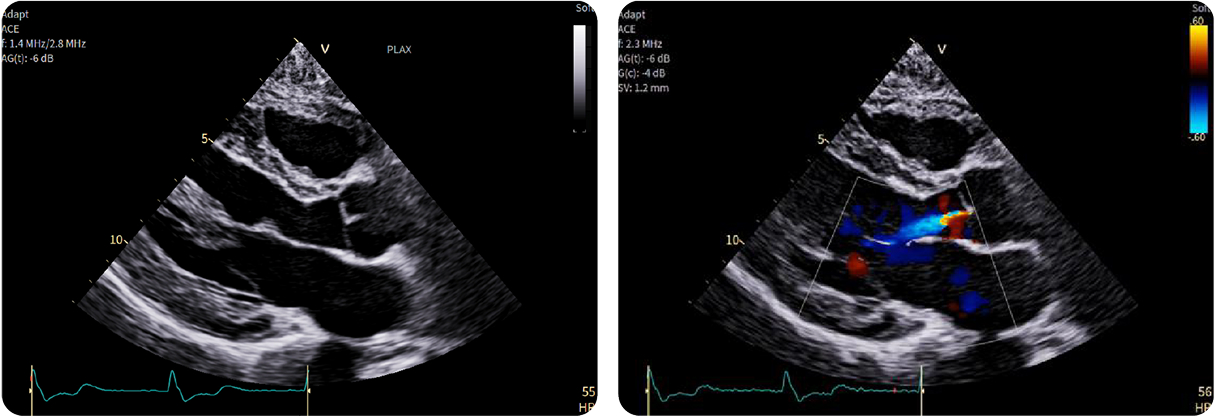 1. Ecocardiografia 2D: asse lungo parasternale
1. Ecocardiografia 2D: asse lungo parasternaleIpertrofia ventricolare sinistra (IVS) con segni di pregressa miectomia settale, ipertrofia dei muscoli papillari, assenza di movimento sistolico anteriore (SAM) (sinistra)
Lieve rigurgito mitralico centrale, lieve rigurgito aortico centrale (destra)
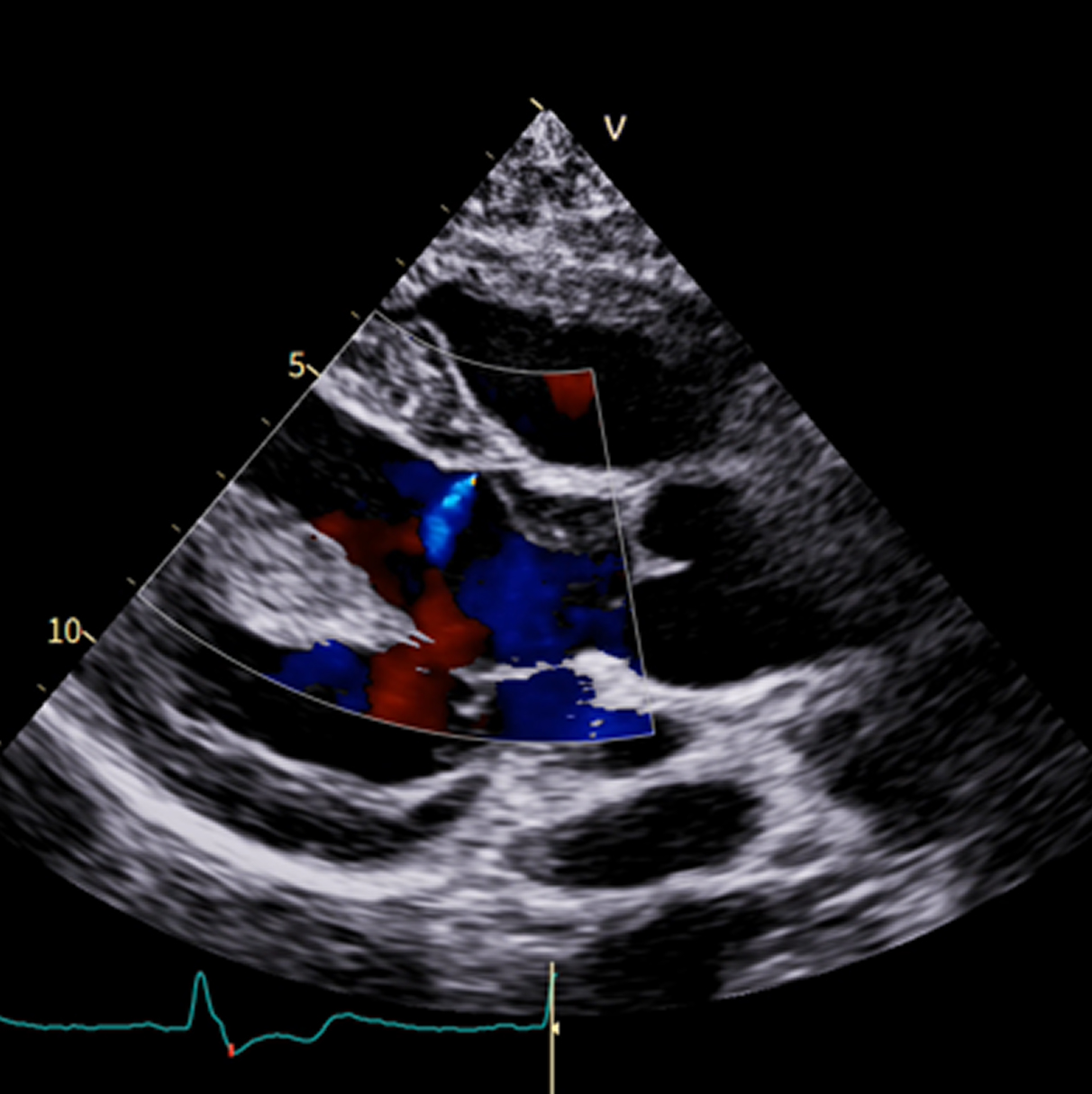
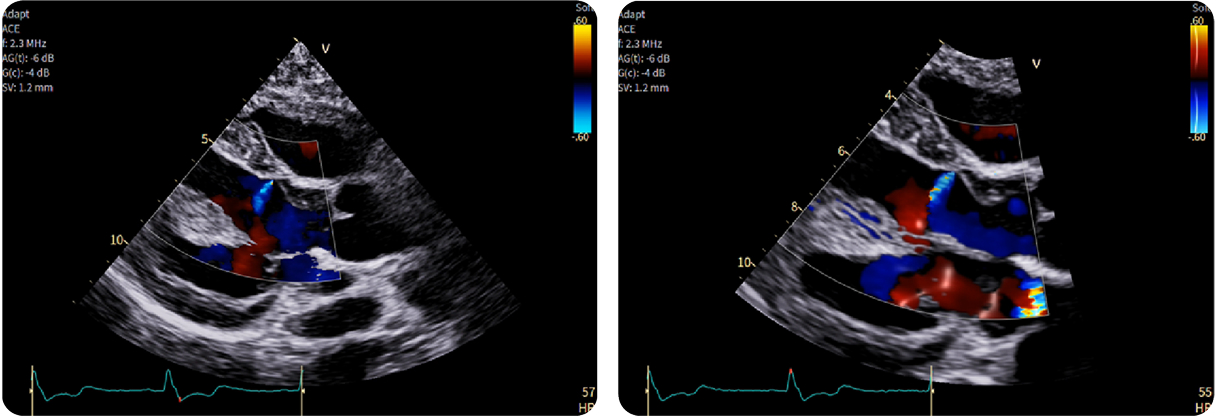 2. Ecocardiografia 2D: Color Doppler e Radiantflow™
2. Ecocardiografia 2D: Color Doppler e Radiantflow™Sottile flusso di getto diastolico tra il setto interventricolare (IVS) e la cavità del ventricolo sinistro (sinistra)
Radiantflow - per valutare meglio la direzione del flusso (destra)
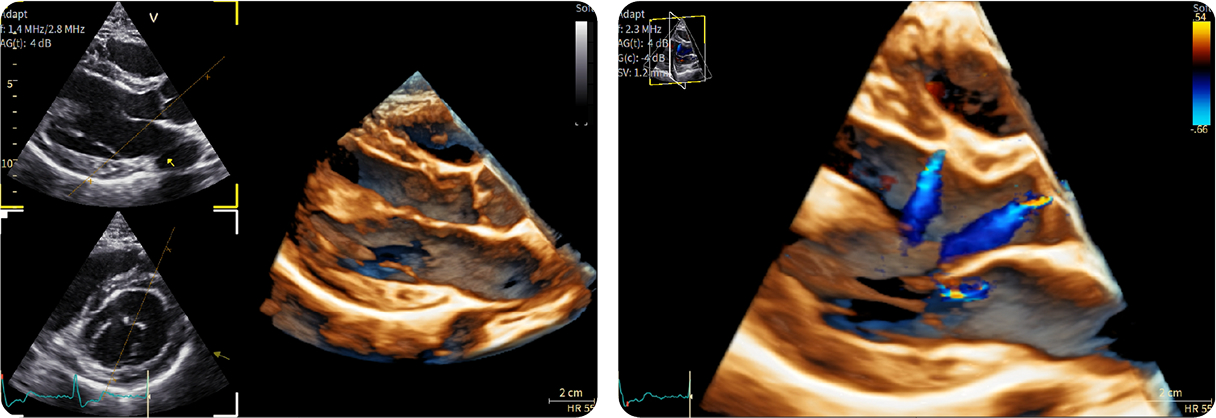 3. Ecocardiografia anatomica 4D e Color Doppler
3. Ecocardiografia anatomica 4D e Color DopplerAssottigliamento residuo del setto interventricolare dopo miectomia (6 mm) – assenza di SAM – ipertrofia dei muscoli papillari (sinistra)
Tre differenti lesioni evidenziate al Color Doppler nella stessa immagine, in acquisizione a singolo battito (destra)
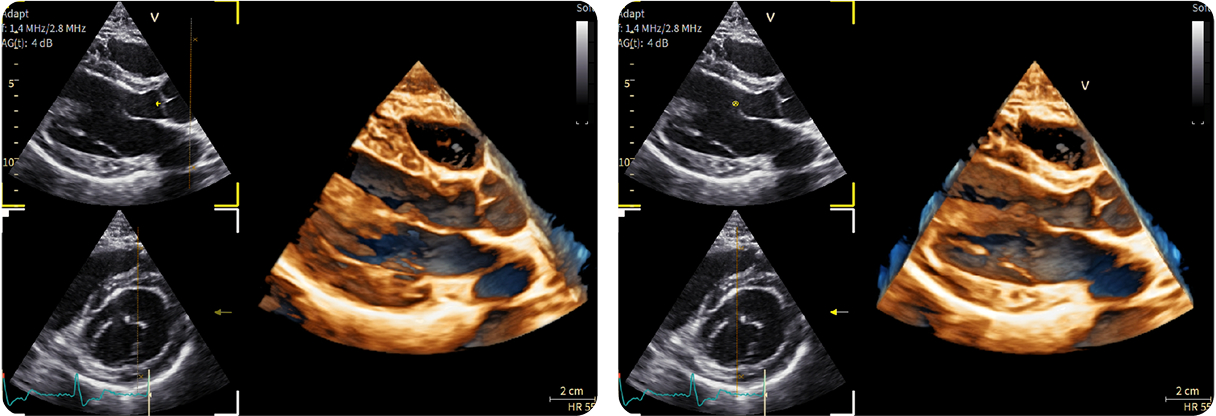 4. Ecocardiografia 4D per superare i limiti della sola 2D
4. Ecocardiografia 4D per superare i limiti della sola 2DAssottigliamento residuo del tratto anteriore del setto interventricolare (IVS) dopo miectomia (sinistra)
Non si evidenziano l’assottigliamento residuo né l’origine della fistola (destra)
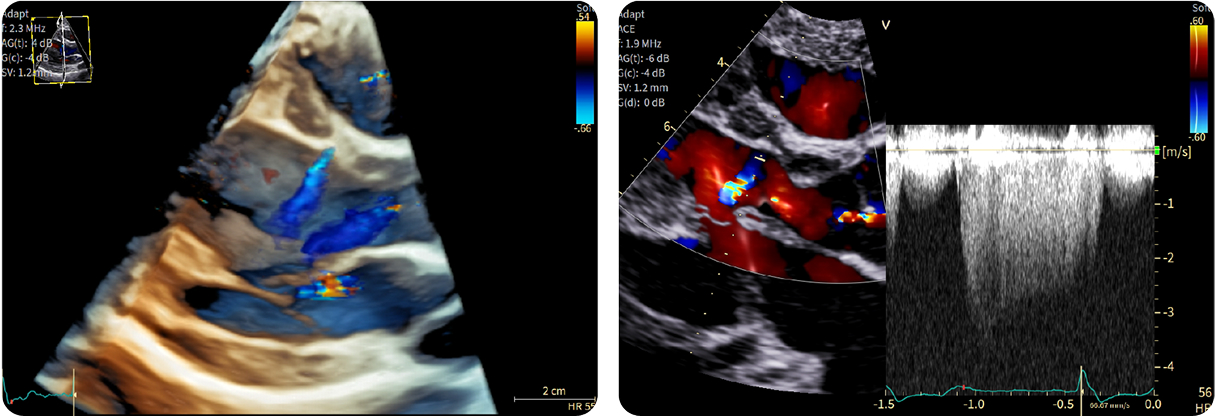 5. Color e CW Doppler 4D per migliore definizione spaziale e temporale
5. Color e CW Doppler 4D per migliore definizione spaziale e temporaleRotazione cine per documentare meglio la localizzazione e l’origine del jet (sinistra)
Doppler CW per documentare meglio la direzione e la temporizzazione del jet (destra)
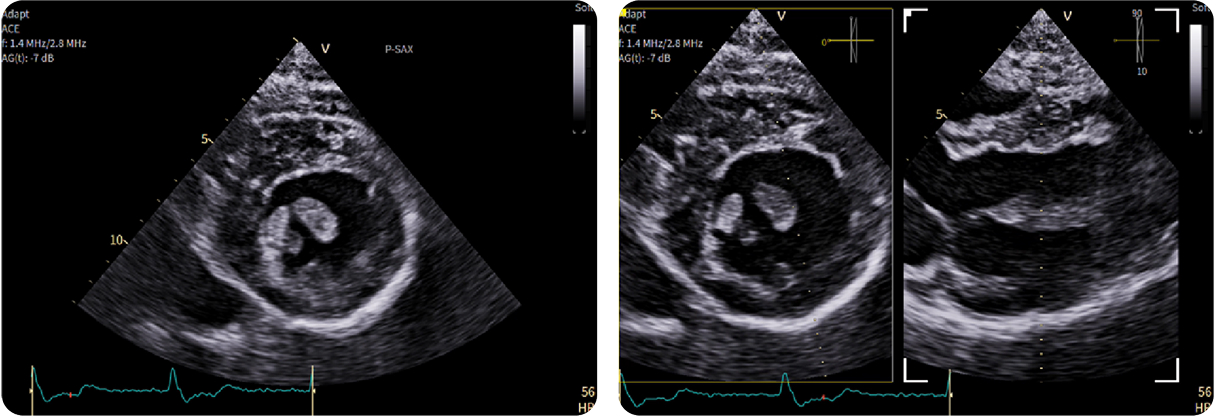 6. Ecocardiografia 2D: asse corto parasternale e biplano
6. Ecocardiografia 2D: asse corto parasternale e biplanoMuscolo papillare postero-mediale bifido – muscolo papillare antero-laterale dislocato con contatto sistolico – assenza di assottigliamento settale (sinistra)
Visualizzazione biplanare dell’ipertrofia dei muscoli papillari (destra)
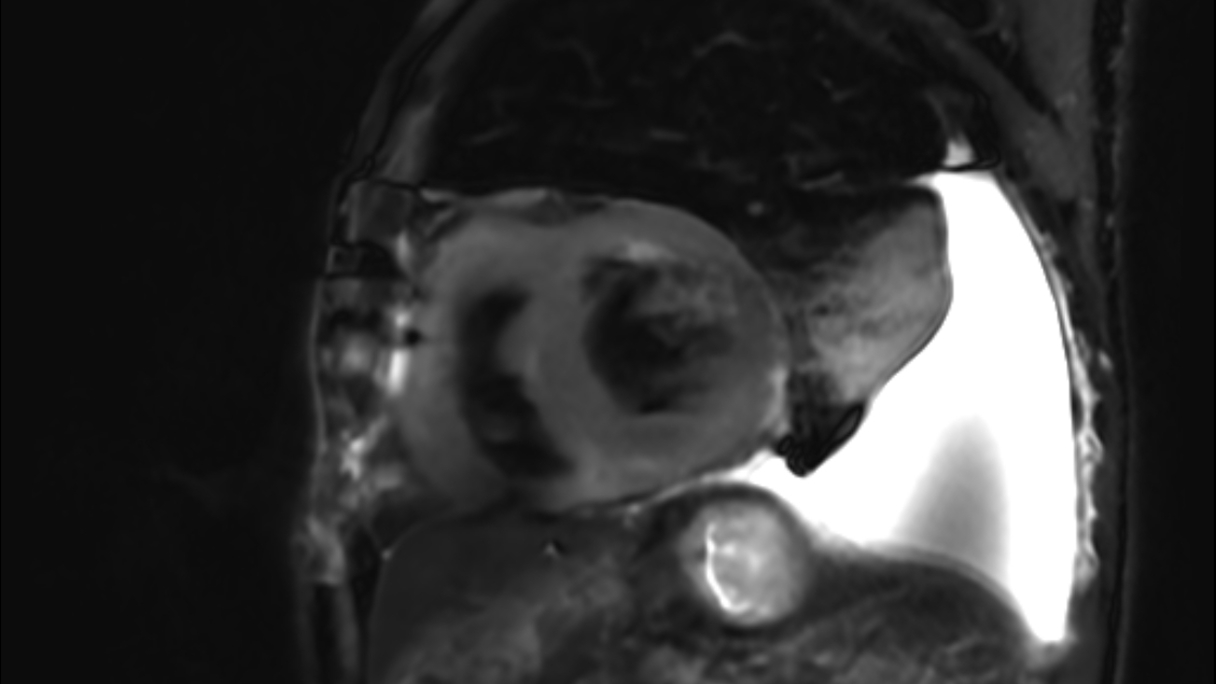
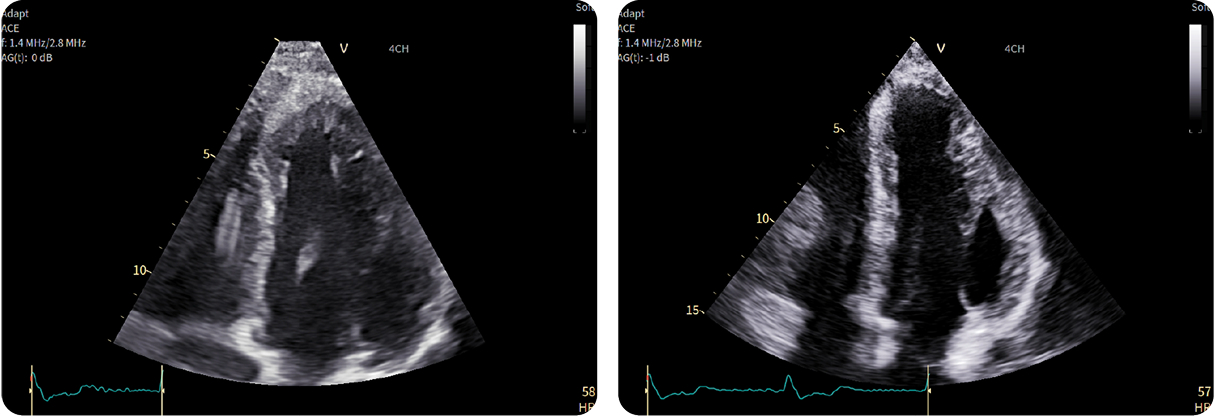 7. Ecocardiografia 2D: viste apicali
7. Ecocardiografia 2D: viste apicaliCardiomiopatia ipertrofica apicale dovuta ad accorciamento apicale del ventricolo sinistro nella proiezione apicale 4 camere in 2D (sinistra)
Aneurisma apicale associato a ipertrofia medio-ventricolare e dei muscoli papillari (destra)
Storia clinica del paziente/patologia
- Paziente maschio di 53 anni con Cardiomiopatia Ipertrofica (HCM) e ostruzione apicale-medio-ventricolare (MVO), anamnesi di miectomia chirurgica e aneurismectomia apicale (2015), con impianto di ICD (2020)
- Ultima CMR (2020, prima dell’ICD): nessun aneurisma residuo del ventricolo sinistro, LVEF 55%, pertanto sospensione della terapia anticoagulante
- Follow-up ecocardiografico in altra sede: dimensioni ventricolari normali, funzione sistolica stabile (LVEF 2D = 60%), assenza di gradiente intracavitario residuo, indicativo di esito ottimale post-procedura
- Persistenza di sintomi: dispnea da sforzo (NYHA II), lieve riduzione della capacità funzionale, NT-proBNP elevato (643). Terapia: beta-bloccante, ACE-inibitore, statina
Criticità
- Pregressa sternotomia
- ICD non compatibile con CMR
Sistema, sonda e dispositivi utilizzati
- Vivid™ Pioneer
- Sonda 4Vc-D
- Sonda 6Sc-D
Procedura step‑by‑step
- Ecocardiografia 2D e 4D completa (sonda 4Vc-D)
- Imaging ecocardiografico apicale mirato (sonda 6Sc-D)
Conclusioni
- HCM post-miectomia chirurgica con aneurisma apicale e ostruzione dinamica residua a livello apicale-midventricolare dovuta a ipertrofia dei muscoli papillari
- Presenza di fistola iatrogena coronaria-cavità ventricolare da confermare con metodica di seconda linea (tipicamente TC coronarica)
- Lieve dilatazione ventricolare sinistra con disfunzione sistolica lieve
- Atrio sinistro moderatamente dilatato
- Rigurgito mitralico lieve
- Rigurgito aortico lieve
- Rigurgito tricuspidale lieve associato a lead ICD (senza interferenze) con dimensioni e funzione ventricolare destra normali
Imaging follow-up
- Reintroduzione di NOAC e ottimizzazione della terapia per scompenso
- Programmazione di eco da sforzo e CPET per valutare in modo oggettivo la causa dei sintomi e la compromissione funzionale
- TC coronarica per valutare la fistola e pianificazione di valutazione emodinamica invasiva
- Discussione multidisciplinare per valutare indicazione a chiusura percutanea
Feedback complessivo
- Qualità d’immagine eccellente con risoluzione spaziale e temporale migliorata nelle immagini 4D
- Elevata sensibilità nel rilevare piccoli jet color Doppler
- Capacità di apprezzare dettagli anatomici fini delle strutture intracavitarie, rilevanti per diagnosi e gestione dell’HCM
- Integrazione efficiente di funzionalità 2D/4D/Doppler, sonde e tecniche ecografiche per una valutazione anatomica e funzionale completa
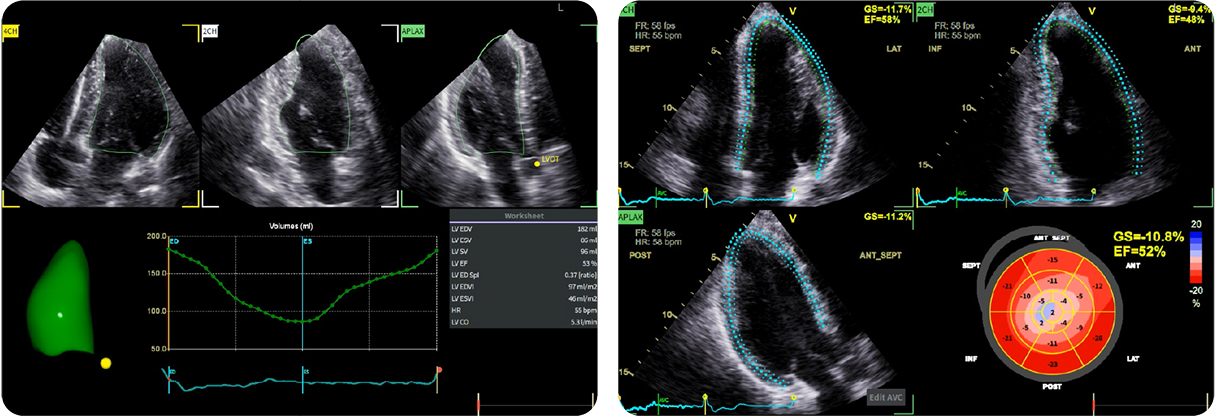
La chiara visualizzazione dei contorni parietali, estesa fino alla porzione più distale del miocardio, consente di apprezzare i dettagli anatomici e le trabecolazioni e aiuta a confermare l’eventuale presenza di ostruzione a livello medio-cavitario, includendone sede e meccanismo
La tecnica 4D LHQ ha rivelato che il paziente presentava già una disfunzione del ventricolo sinistro (FE VS 53%, VTD VS 162 ml). La presenza della fistola potrebbe potenzialmente aggiungere un ulteriore carico emodinamico a un ventricolo già compromesso da fibrosi e ipertrofia ventricolare sinistra
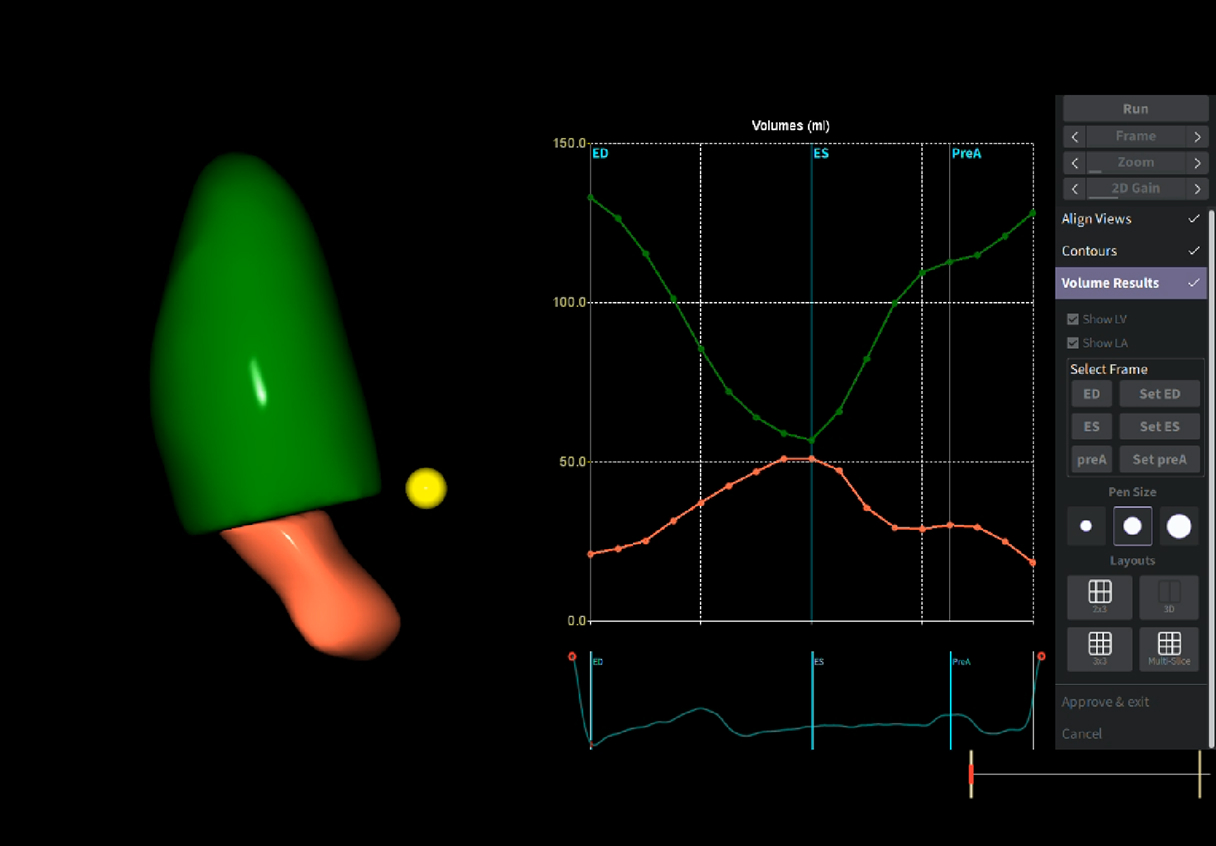
La 4D LHQ consente l’acquisizione e la misurazione simultanea del ventricolo sinistro (VS) e dell’atrio sinistro (AS), permettendo la valutazione del loro accoppiamento, un parametro importante per predire la presenza di fibrillazione atriale nei pazienti con cardiomiopatia ipertrofica
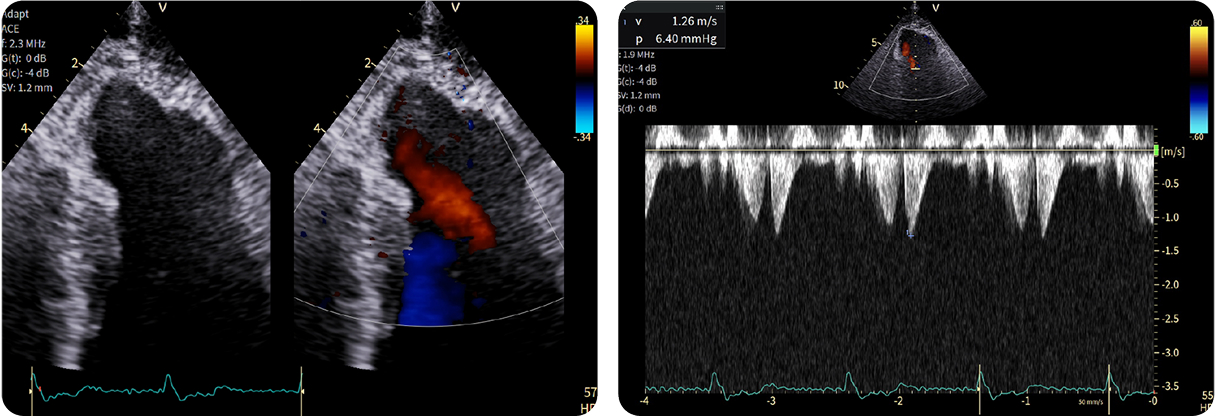
Color Doppler con flusso bifasico proveniente dall’aneurisma (sinistra)
Doppler CW con segno a “chela di aragosta” (destra)
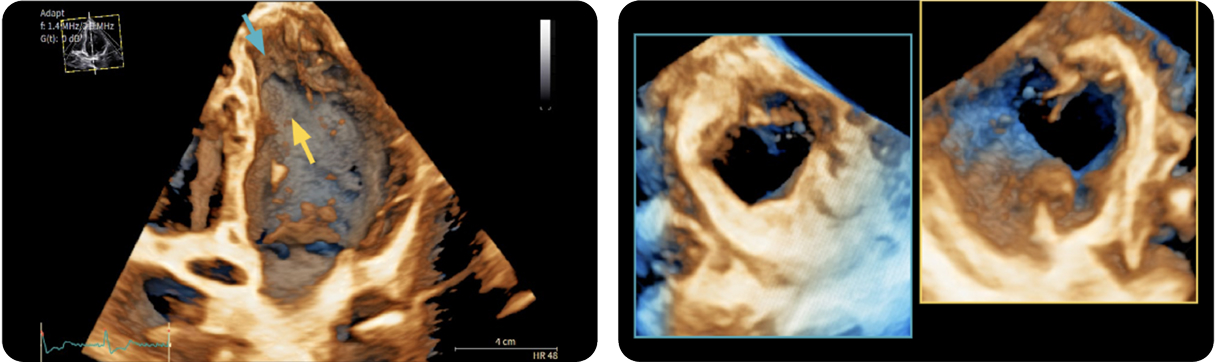
Ostruzione dinamica del ventricolo sinistro (sinistra)
Dual-Crop Ventricolo Sinistro (destra)
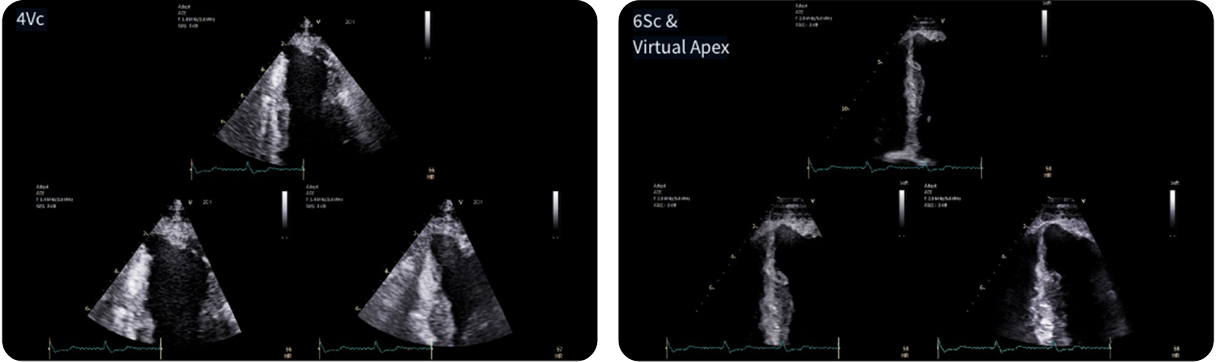
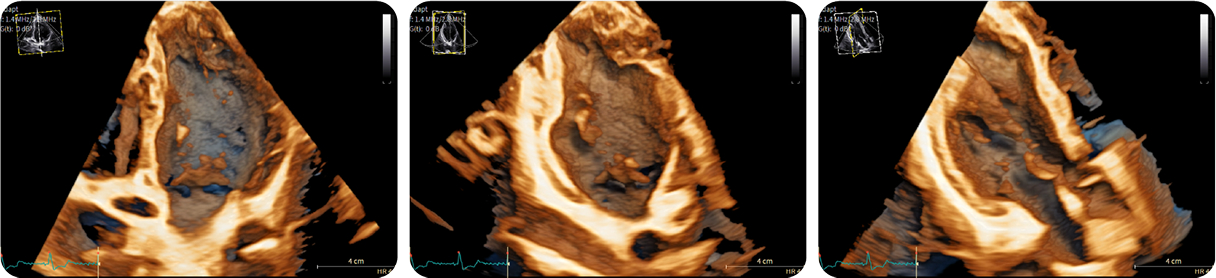
Il confronto tra la sonda ad alta frequenza 4Vc‑D e la 6Sc‑D ha dimostrato che quest’ultima consente una chiara visualizzazione dell’apice, confermando l’assenza di trombo intracardiaco
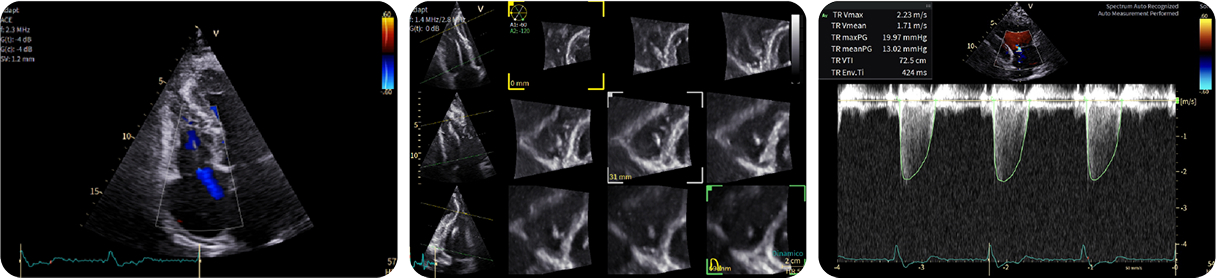 14. Valutazione del meccanismo e della severità del rigurgito tricuspidale
14. Valutazione del meccanismo e della severità del rigurgito tricuspidaleLa chiara visualizzazione dei contorni parietali, estesa fino alla porzione più distale del miocardio, consente di apprezzare i dettagli anatomici e le trabecolazioni e aiuta a confermare l’eventuale presenza di ostruzione a livello medio-cavitario, includendone sede e meccanismo
Vuoi approfondire il caso con un nostro esperto?